Большинство роботов-хирургов — вовсе не роботы в классическом понимании этого слова. Они «глупы», несамостоятельны и работают по принципу master/slave, или, если политкорректно, — «ведущий-ведомый».
Все они, по сути, марионетки в руках хирурга, сложные инструменты, которые повторяют человеческие движения. Просто имейте это в виду. Название робот-хирург намертво приклеилось к хирургическим манипуляторам даже в научной литературе, так что я буду его использовать несмотря на неточность.
При этом, хирургическая робототехника начиналась именно с программируемых машин и лишь затем свернула на другую дорожку.
Пятиминутка навигации
Внимание, здесь рассказывается о хирургии. В статье нет шок-контента, но если у вас живое воображение, вы это, поаккуратнее.
- Если вам интересно, откуда растут ноги у хирургических роботов, читайте по порядку.
- Ниже рассказано, как работают хирургические манипуляторы, и зачем они вообще понадобились в операционной.
- Дальше — большой раздел для любителей техники. Потроха и схемы самых популярных роботов-хирургов прилагаются.
- В четвертой части статьи вы узнаете, что не так со всеми этими железками.
- В пятой — почему так сложно сделать «рободока», прямо как в фантастическом фильме.
- И под конец о хорошем, о том, какие технологии в обозримом будущем сделают роботов-хирургов на порядок полезнее и эффективнее.
Первый среди ранних
В 1985 году 52-летнего мужчину поместили в компьютерный томограф. Ему вскрыли череп и ввели в мозг тонкую иглу для забора образца ткани. В этой операции хирургам помогал манипулятор PUMA 200, созданный для работы на конвейерах General Motors. Это было первое применение робота в хирургии.


Промышленный манипулятор понадобился для точного позиционирования и удержания направляющей трубки, через которую вводилась игла.
Операция закончилась благополучно, но производитель робота не оценил самодеятельность и запретил использовать PUMA в хирургии. Скорее всего, из-за репутационных и юридических рисков. Вы бы тоже побоялись однажды прославиться, как производитель роботов-убийц.
ROBODOC
Уже на следующий год ветеринар Говард «Хэп» Пол и инженер Уильям Баргар вместе со спецами из IBM запустили разработку робота для эндопротезирования суставов.

Раньше имплантаты «приклеивали» на акриловый цемент. Он постепенно разрушался, и вскоре пациенты снова отправлялись под нож. В середине 80-х появилась альтернатива — пористые имплантаты. Кость срастается с ними и новый сустав служит десятки лет. Тем дольше, чем меньше зазор и выше точность при установке.
Чтобы делать выемки в кости под установку имплантатов, Пол и Баргар фактически переизобрели фрезерный станок с ЧПУ. Они назвали его ROBODOC, ага, в честь Робокопа.

Как вы могли догадаться, сначала ROBODOC испытали на собаках с травмами бедра, а затем и на людях под надзором Food and Drug Administration (FDA) — подразделения минздрава США и настоящего ночного кошмара медицинских стартапов.
Конструктивно, Robodoc — это 5-осевой манипулятор SCARA, на конце которого закреплена режущая головка с 6-осевым датчиком давления и системой подачи воды для охлаждения и удаления пыли.
Перед операцией ногу пациента жестко фиксируют при помощи винтов. Их вкручивают прямо в кость. К кости привязывается координатная сетка, в которой действует робот. Программу операции готовят заранее на базе трехмерной модели, созданной при помощи компьютерной томографии.
У конструкторов ROBODOC получилось добиться высокой точности реза, до 0,5 мм. В результате, робот снимал лишь на 0,54% больше ткани, чем необходимо. Это при том, что при ручной установке имплантата хирурги удаляли примерно на 30% больше кости.
Казалось бы, вот он — успех, но клинические испытания затянулись. В 1994 году ROBODOC стал первым хирургическим роботом, допущенным на рынок ЕС, но вскоре использование машины остановили из-за череды несчастных случаев.

Доработки и повторные испытания закончились только в 2008 году. Только тогда ROBODOC наконец получил одобрение FDA. Можно только позавидовать упорству его создателей. Долгое время он был единственной программируемой хирургической системой, которую разрешено использовать в США.
В дело вступают военные
В числе первых людей, заинтересовавшихся медицинской робототехникой, были и военные инженеры из американского оборонного агентства DARPA. Пока ROBODOC тренировался на кошках, фрезеровал собак, они раздумывали над концепцией телехирургии.
Пожалуй, самая гуманная из их идей, тогда казалась очень перспективной. При помощи робота с дистанционным управлением хирурги могли бы оперировать раненных неподалеку от линии фронта, не отвлекаясь на пули, свистящие над головой.
Военные разыскали проекты дистанционных манипуляторов NASA и кое-какие прототипы, спроектированные для космоса в Стэнфордском научно-исследовательском институте (SRI). Большая часть наработок базировалась на чисто механических манипуляторах, созданных еще для Манхэттенского проекта, и малость устарела. Так что пришлось объявлять конкурс и раздавать гранты.
DARPA финансировало исследования телехирургии без малого десять лет, вплоть до 90-х годов прошлого века. Выяснилось, что при задержке сигнала более 200-300 мс хирургическое вмешательство становится затруднительным, а при 700 мс лишь очень немногие хирурги в состоянии выполнить свою задачу (а вы еще жалуетесь на пинг в компьютерных играх). Тогда военные решили, что не могут обеспечить необходимую скорость связи, и заморозили программу.


И все же, благодаря DARPA появились две частных компании, которые поставили себе более реалистичную цель — создание системы для роботизированной малоинвазивной хирургии безо всякого телеприсутствия.
Эзоп и Зевс
Один из последних грантов DARPA достался кандидату наук из Калифорнийского университета в Санта-Барбаре Юлану Вангу. На эти деньги Ванг в 1992 году сконструировал AESOP — роботизированный лапароскоп. Через два года это устройство получило голосовое управление. Теперь лапароскопические операции можно было проводить без помощи живого ассистента.
Как только DARPA остановила исследования, Ванг открыл компанию Computer Motion, Inc. Так на рынке хирургической робототехники появился первый серьезный игрок.
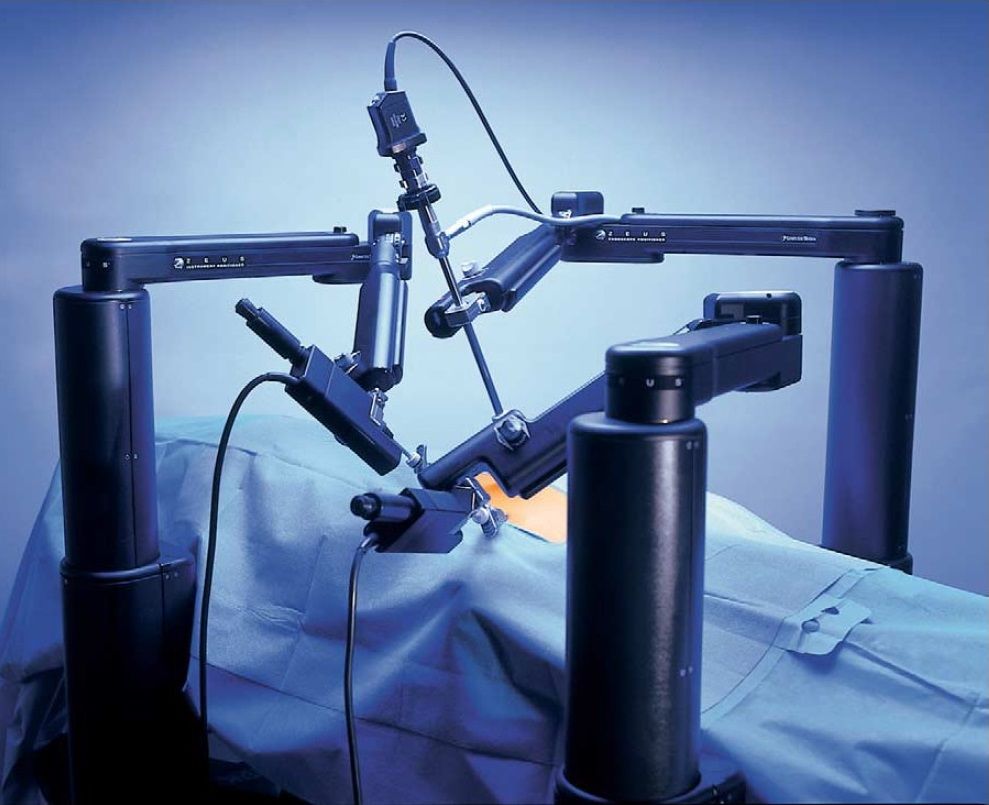
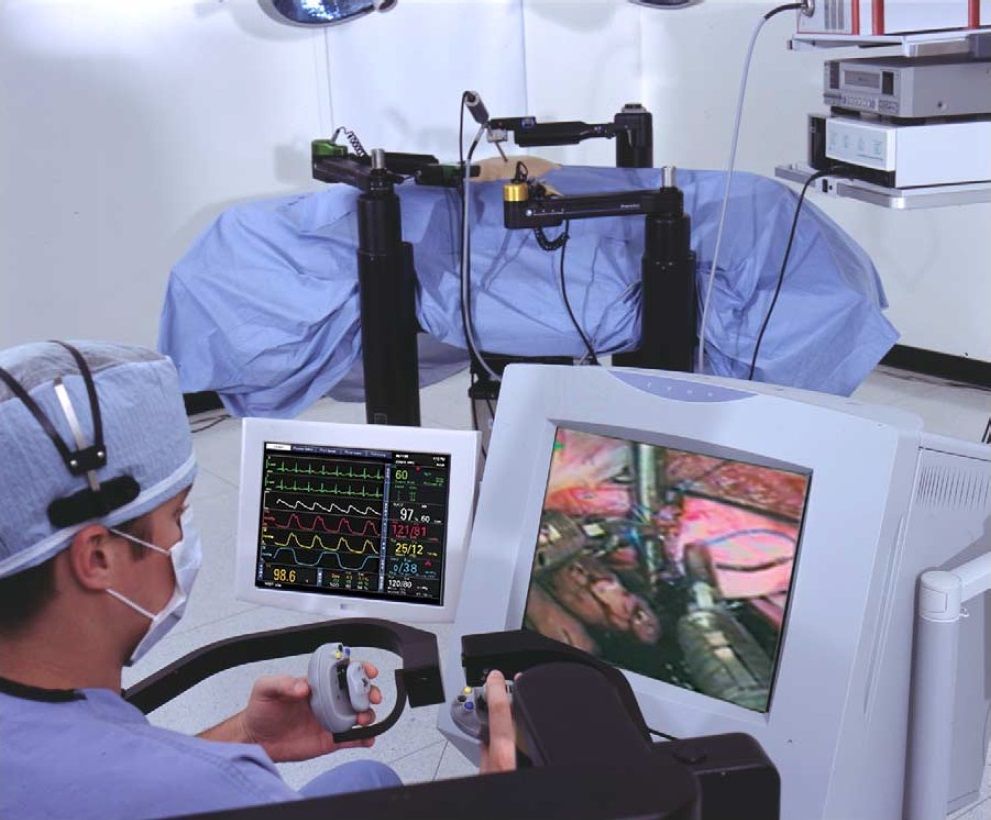
FDA одобрила продажи AESOP в 1994 году, а 1995 году Computer Motion начала испытания трехрукого ZEUS — уже вполне сложившейся хирургической системы типа ведущий — ведомый.
Предки Да Винчи
Пока Ванг трудился над AESOP, студент MIT Ахил Мадхани смотрел сериал про будни военных врачей. Под впечатлением от увиденного, он решил сделать дистанционную хирургию темой своей диссертации.
В 1993 году с помощью профессора Кеннета Солсбери он собрал телеманипулятор Black Falcon. Этот проект тоже профинансировало DARPA.


Прототип так и пылился бы в лаборатории, но в 1995 году хирург Фредерик Молл, венчурный инвестор Джон Фройнд и инженер Роберт Янг основали компанию Intuitive Surgical.
Они начали с того, что скупили все патенты, связанные с дистанционной хирургией, до которых смогли дотянуться: исследования SRI, технологии IBM и разработки MIT. Black Falcon оказался самым полезным из приобретений.

Разработка Мадхани легла в основу прототипов Lenny и Mona (на фото слева), а затем и манипуляторов робота-хирурга da Vinci первого поколения.
Зевс против Да Винчи (в кинотеатрах вашего города)
Испытания ZEUS начались раньше, но da Vinci первым вышел на рынок США. Робот поступил в продажу в 2000 году по цене чуть более 1 млн долларов. ZEUS получил одобрение FDA в октябре 2001 года и на старте продавался по цене 975 тыс долларов. ZEUS был меньше и дешевле, а da Vinci — ловчее.
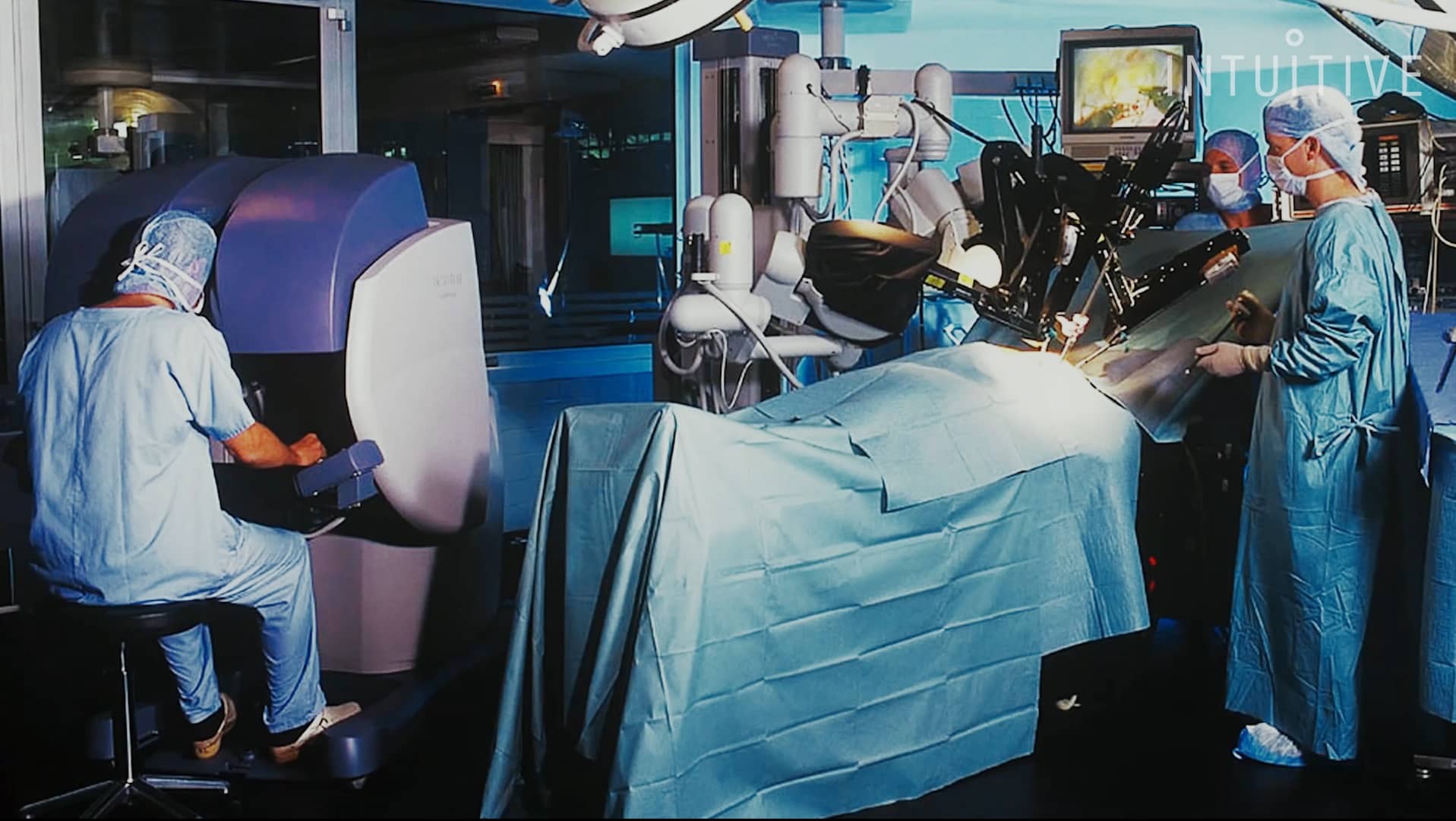
Сперва da Vinci рекламировали как специализированное устройство для тонкой кардиохирургии, но роботом заинтересовались урологи и гинекологи, вынужденные работать в стесненной и заполненной различными органами тазовой полости.
Основатели Intuitive Surgical иногда шутят, что при разработке da Vinci компания целилась в сердце, а попала в простату
С их подачи FDA разрешила использовать da Vinci в малоинвазивной хирургии таза. В то же время Computer Motion подала в суд на растущего конкурента. Юристы сцепились намертво, разбирательство затянулось, убытки росли, и, в конце концов, компании договорились о слиянии. ZEUS вывели из эксплуатации в пользу da Vinci.

С тех пор этот робот-хирург остается наиболее популярным, и несколько новых систем копируют его конструкцию. По данным на 31 марта 2021 года Intuitive Surgical установила уже 6 142 робота разных поколений по всему миру. Список процедур, в которых применяется da Vinci, растет до сих пор.
Причины популярности
Чтобы понять, почему da Vinci так приглянулся хирургам, нужно знать, что представляет собой лапароскопическая, она же малоинвазивная хирургия.
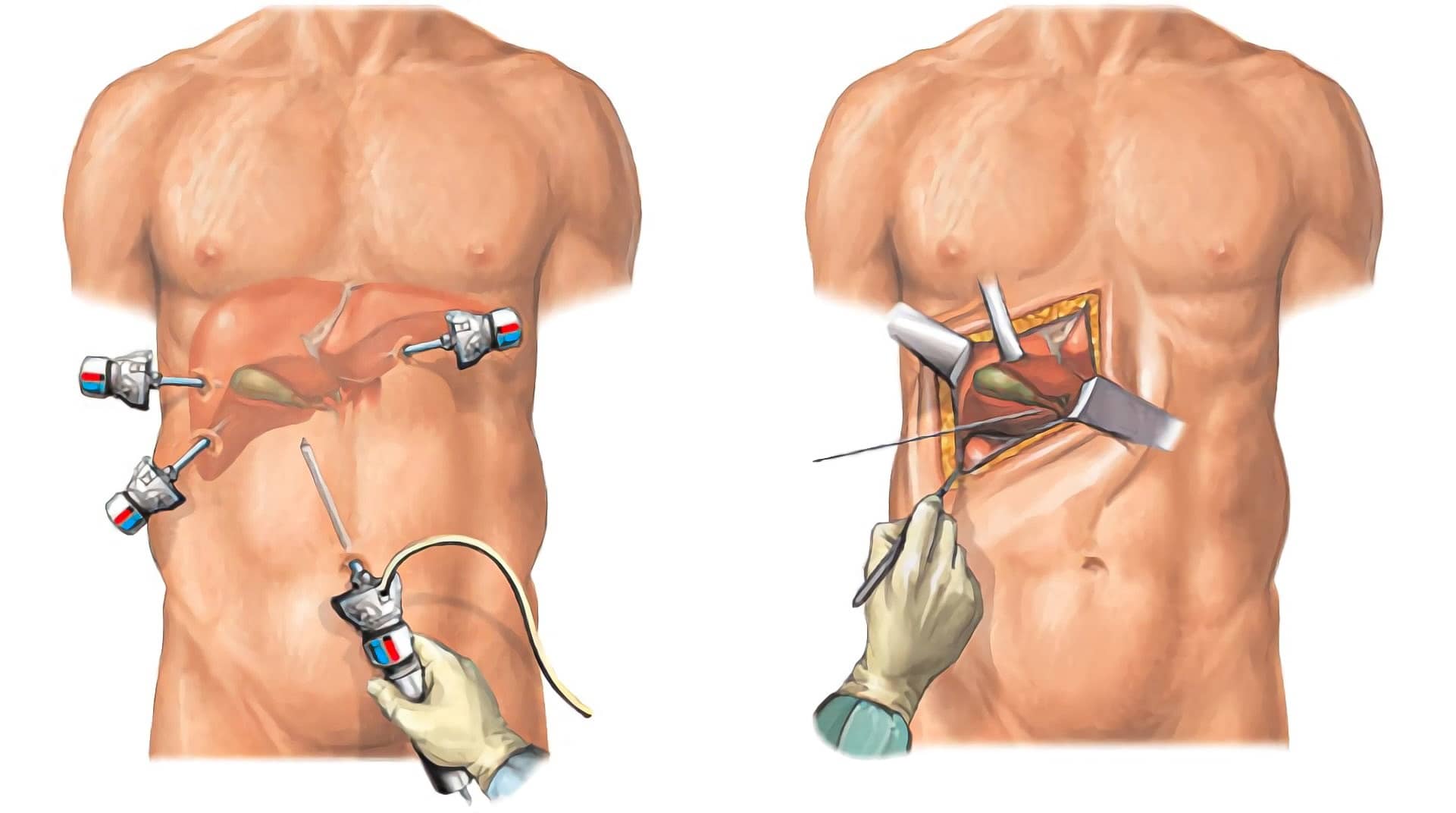
Во время такой операции, например, на печени, сперва в районе пупка делается небольшой разрез, через который вставляется эндоскоп, состоящий из камеры с подсветкой и канала для подачи углекислого газа. Газ наполняет брюшную полость, как воздушный шарик, и у хирурга появляется пространство для работы.
В то же время в боковой части живота делается еще пара небольших разрезов. В них вставляются троакары — металлические трубки с обратным пневматическим клапаном. Через них в организм вводятся хирургические инструменты, закрепленные на концах длинных стержней: ножницы, пинцеты и мешочки, куда можно положить все, что нужно вынуть из организма.
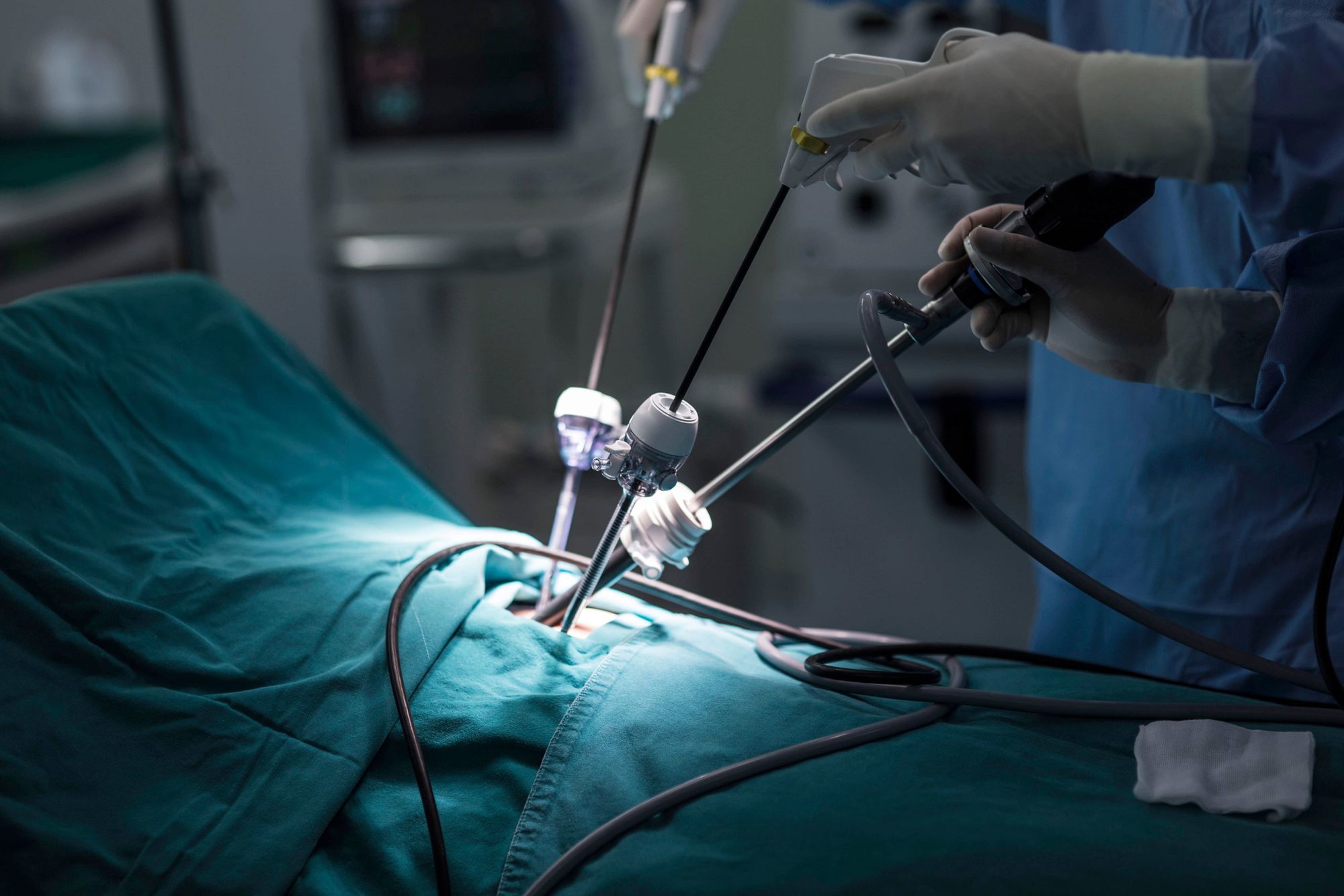
Такой подход сильно сокращает «сопутствующий ущерб». Пациенты, которые обычно занимают больничные койки неделями после операции, отправляются домой уже через пару дней и почти без шрамов.
Это замечательно, вот только малоинвазивная хирургия — чертовски сложное дело. Хирурги говорят, что такие операции похожи на сборку кораблика в бутылке при помощи палочек для еды. Дело в том, что инструменты вводятся в организм через отверстие не больше сантиметра диаметром, а их рабочий конец отделен от рукоятки 30 см валом, который усиливает дрожание наконечника.
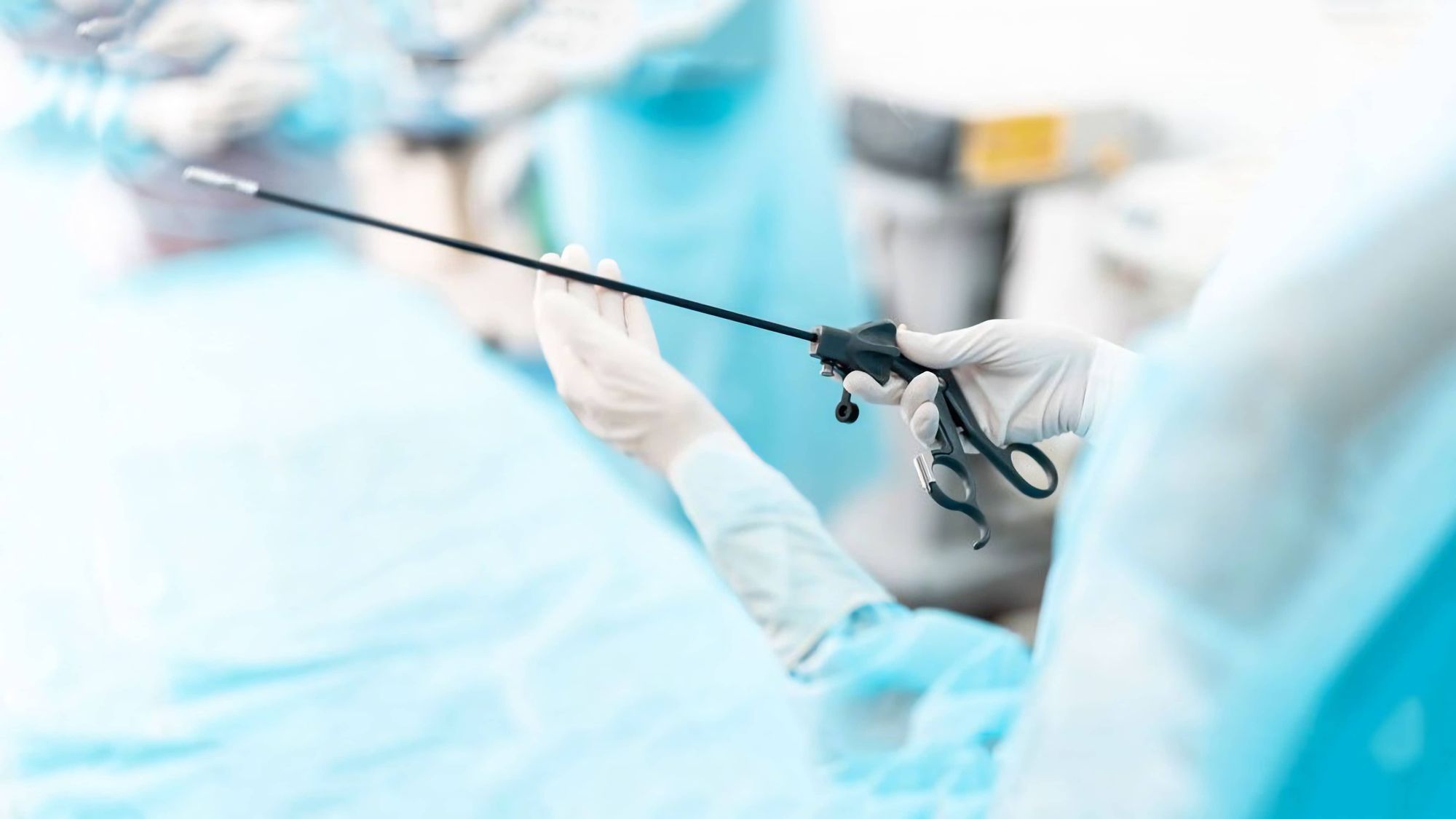
Кроме того, возникает эффект точки опоры — при перемещении рукоятки инструмента вниз, наконечник поднимается, и наоборот. В результате, хирург вынужден совершать все действия будто в зеркальном отражении. Это многократно усложняет обучение и утомляет даже опытных хирургов. В одной из статей об эргономике хирургических роботов метко подмечено, что использование лапароскопических инструментов «снижает когнитивную полосу пропускания» хирурга, замедляет принятие решений.
Не говоря о том, что хирург сильно ограничен в движениях, не может подвести инструмент к цели под произвольным углом и вынужден использовать дополнительные инструменты, чтобы это компенсировать. Наконец, приходится наблюдать за процедурой при помощи лапароскопической камеры, а это означает не лучший обзор и плоскую, двухмерную картинку.
Все это делает сравнительно простые процедуры, вроде наложения швов и завязывания узлов, очень и очень непростой задачей.
Когда на рынок вышли ZEUS и da Vinci, оказалось, что роботы могут делать все то же самое, но управлять ими гораздо проще, чем лапароскопическими инструментами.
При помощи манипуляторов da Vinci хирург оперирует так, будто его руки оказались внутри пациента. Робот полностью избавляет от эффекта точки опоры и позволяет использовать навыки, приобретенные во время открытых операций.
Есть и дополнительные преимущества. Робот фильтрует движения хирурга и снижает дрожание инструментов даже по сравнению с открытой хирургией. Кроме того, da Vinci масштабирует движения, например, 2 к 1 — превращает каждые два сантиметра движения руки хирурга в один сантиметр движения манипулятора.
Общий вид системы и поколения da Vinci

Существует шесть моделей роботов da Vinci:
- оригинальная система 1999 года выпуска;
- da Vinci S 2006 года. У него появился 3D-эндоскоп;
- da Vinci Si 2009 года, получивший поддержку второй консоли для совместных операций;
- версия Xi 2014 года, которая отличается обновленной конструкцией манипуляторов и самым широким набором функций;
- da Vinci X 2017 года — удешевленная модель на базе манипуляторов da Vinci Si и современных инструментов, созданных для версии Xi;
- da Vinci Single port 2018 года. Как можно догадаться по названию, эта версия с единственным манипулятором и одной точкой входа в организм. Продается только в нескольких странах и, вероятно, будет доработана для выхода на мировой рынок.
Все эти телехирургические системы работают по одному принципу и конструктивно схожи (выделяется разве что da Vinci Sp), поэтому рассмотрим их в целом, а о значимых различиях поговорим по ходу статьи.
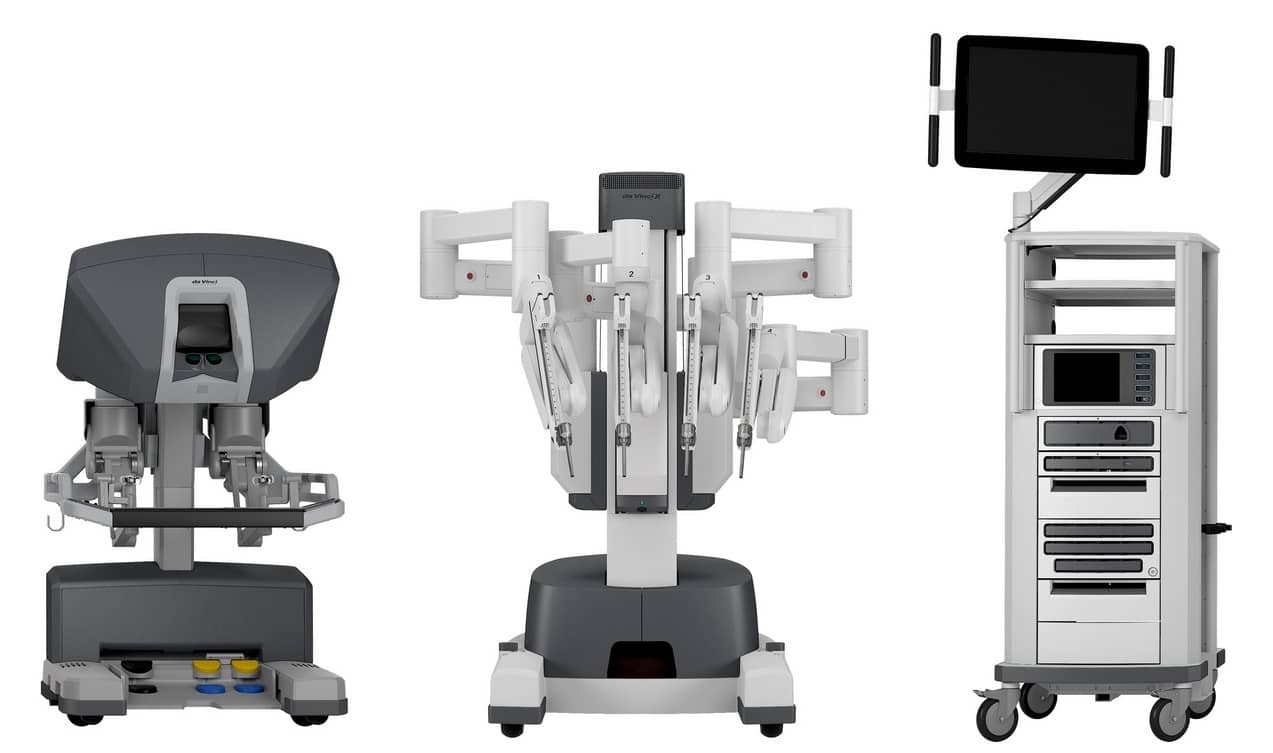
da Vinci состоит из трех отдельных подсистем:
- консоль хирурга — пульт, за которым врач проводит всю операцию;
- консоль пациента — стойка с манипуляторами, которую устанавливают рядом с хирургическим столом;
- видеостойка — там расположены: CORE — ядро — мозг системы, блок обработки картинки с эндоскопа, экран и генератор для электрохирургии.
Консоль хирурга
В теории da Vinci можно использовать для дистанционных операций, но их проводят исключительно редко. Обычно консоль хирурга устанавливают в операционной на расстоянии нескольких метров от пациента, за пределами стерильной зоны.
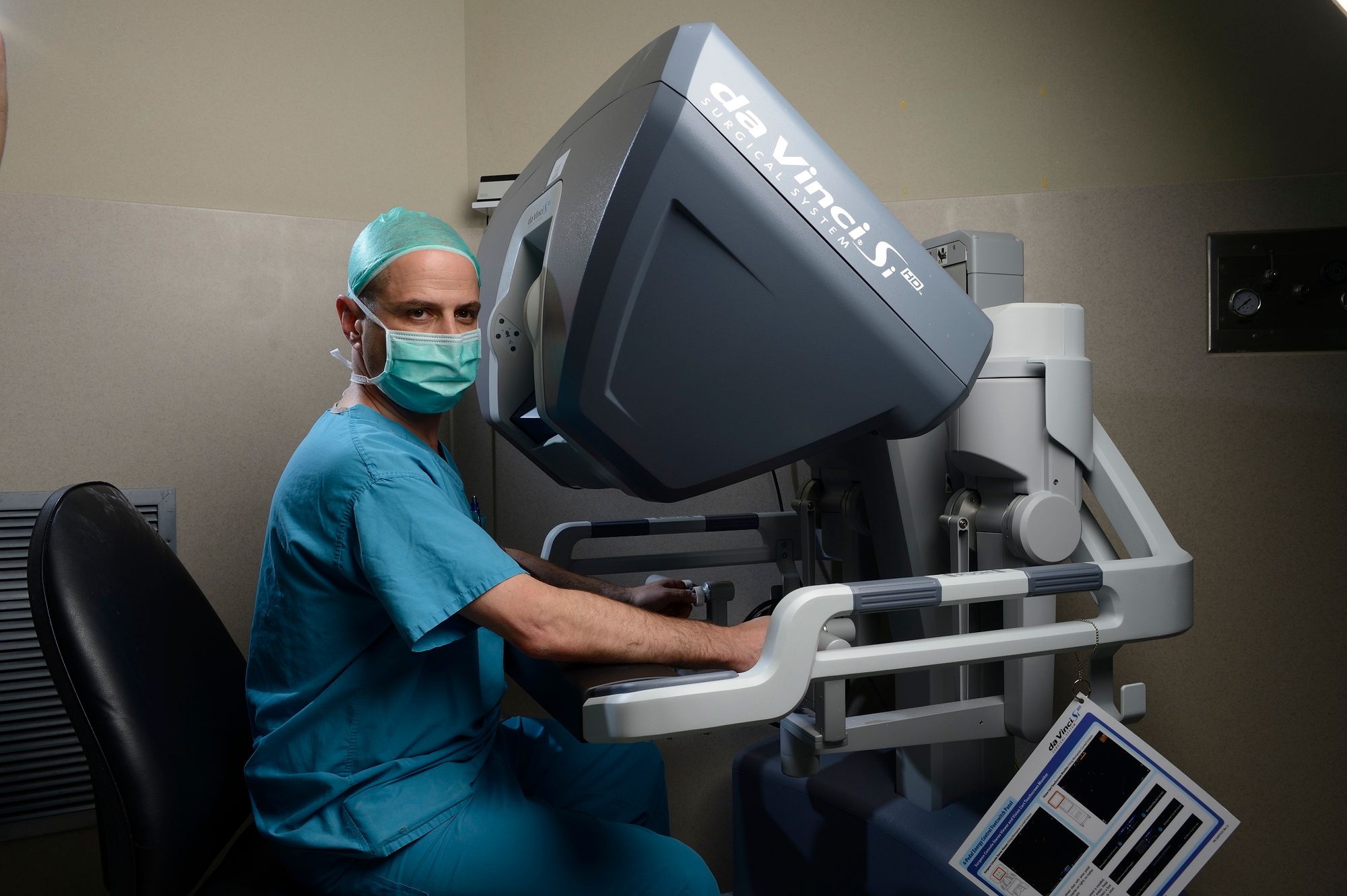
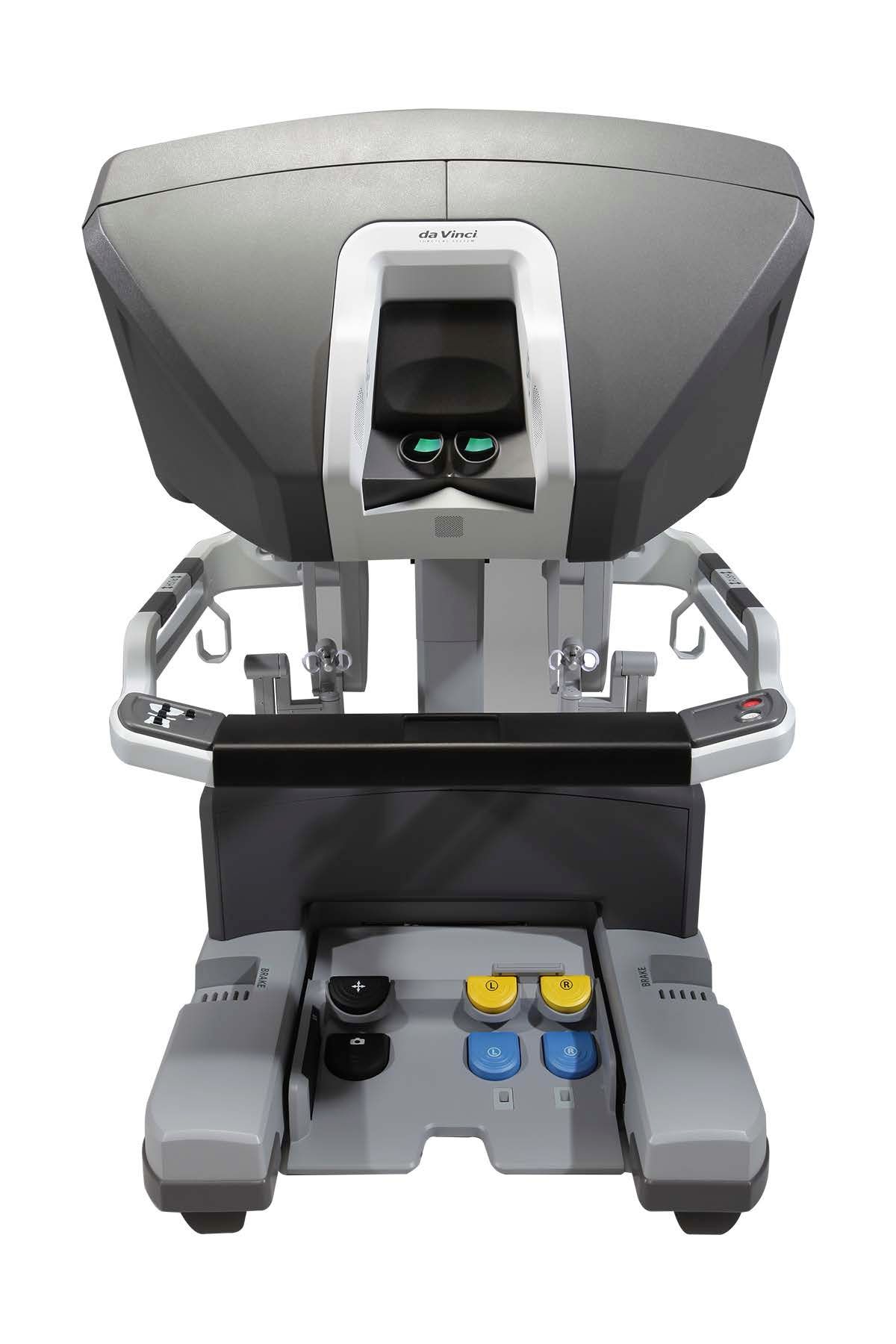
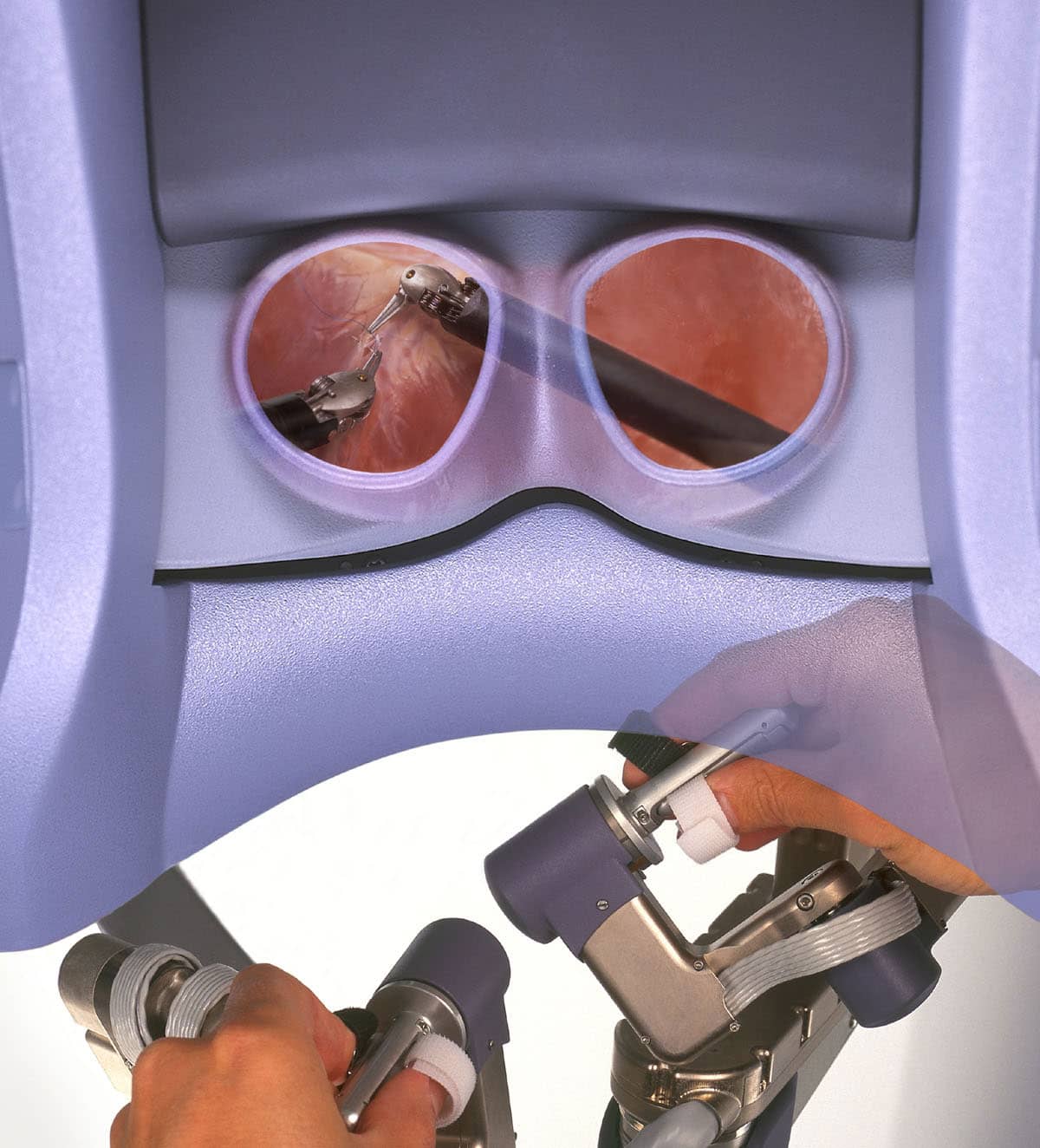
Хирург сидит, склонившись к визору, на который выводится трехмерная картинка с камеры, находящейся внутри пациента. В его поле зрения выводятся пиктограммы и текстовые сообщения, отображающие состояние робота. Туда же можно транслировать изображение с совместимых УЗИ-датчиков и статичные картинки, например, снимки с томографа.

В основе визора пара Full HD-дисплеев. Кстати, консоль снабжена инфракрасным детектором, который блокирует управление роботом, стоит только поднять голову.

В руках хирурга пара контроллеров сложной конструкции, которые в режиме реального времени считывают и передают движения на манипуляторы. Каждая рукоятка состоит из семи последовательно соединенных шарниров.
На конце манипулятора находится «прищепка» с парой регулируемых ремешков, в которые продеваются большой и указательный (или средний) пальцы. Она нужна для того, чтобы, например, открывать и закрывать бранши инструментов. Такая конструкция в сочетании с объемной картинкой в визоре создает ощущение, будто хирург удерживает ткани собственными руками.
Движения не передаются манипуляторам напрямую. В качестве посредника в архитектуре «ведущий-ведомый» выступает компьютер. Ядро снимает показания с шарниров рукояток с частотой больше 1300 раз в секунду, взвешивает, фильтрует от тремора и перечитывает в движения инструментов с учетом габаритов манипуляторов. Человеческие руки дрожат с частотой 6–10 Гц, чтобы отфильтровать колебания, в da Vinci используют фильтр на 6 Гц.
И все же, для управления роботом недостаточно одной пары контроллеров. Как у органа, у консоли хирурга есть еще и педали. Педаль с изображением камеры активирует управление эндоскопом, со стрелками — временно отключает манипуляторы, чтобы хирург мог поставить контроллеры в удобное положение.

Черная боковая педаль слева отвечает за переключение между основными и вспомогательным манипулятором. Желтые и синие управляют различными функциями инструментов, например активируют хирургический степлер.
Консоль пациента и манипуляторы
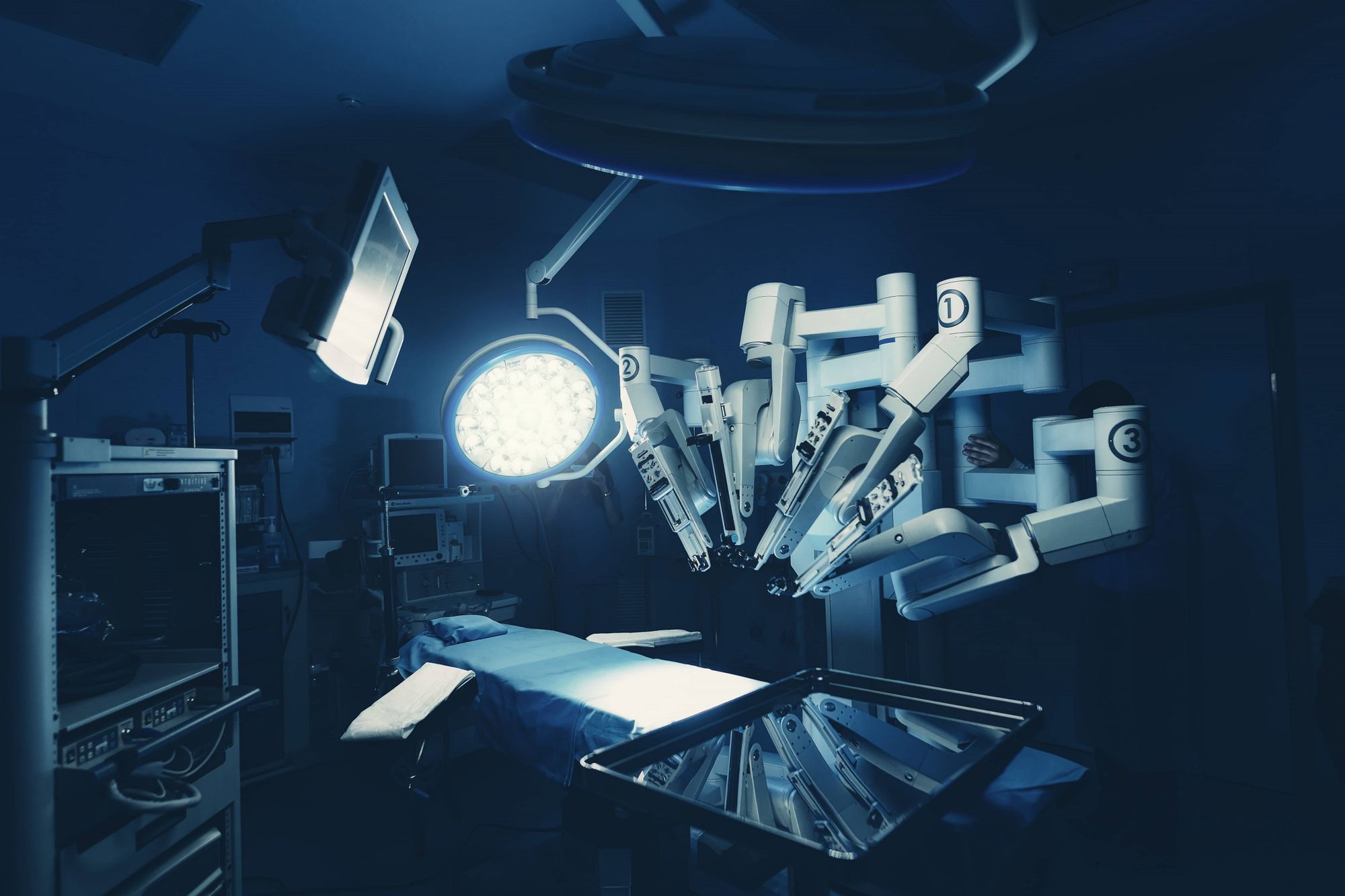
У da Vinci четыре конечности. Как правило, один манипулятор выступает в роли левой руки хирурга — другой — правой. Третий отвечает за картинку — удерживает эндоскоп под нужным углом. Четвертый манипулятор — вспомогательный, он нужен не всегда. С его помощью фиксируют ткани, мешающие работе, или держат наготове инструмент, который понадобится на следующем этапе операции.
Можно сказать, что манипуляторы da Vinci состоят из двух частей: пассивной и активной.
Пассивные манипуляторы
Пассивная часть манипулятора da Vinci X и Si — первые четыре шарнира, расположенные по бокам от колонны консоли. Первый призматический шарнир нужен для регулировки высоты. Следующие три — плоскостные, реверсивные типа SCARA. Они позволяют развести манипуляторы по бокам от пациента так, чтобы они не сталкивались.
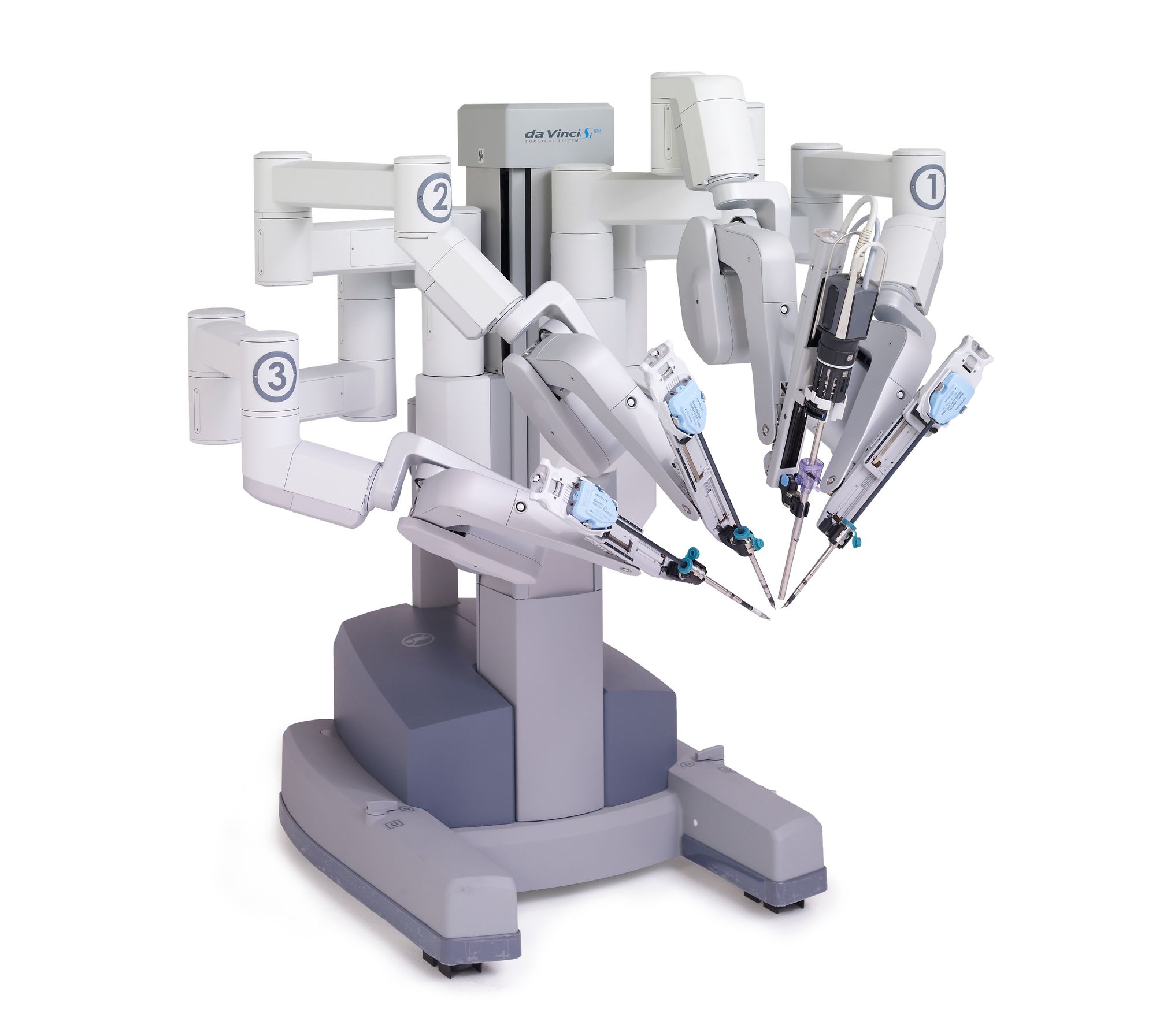
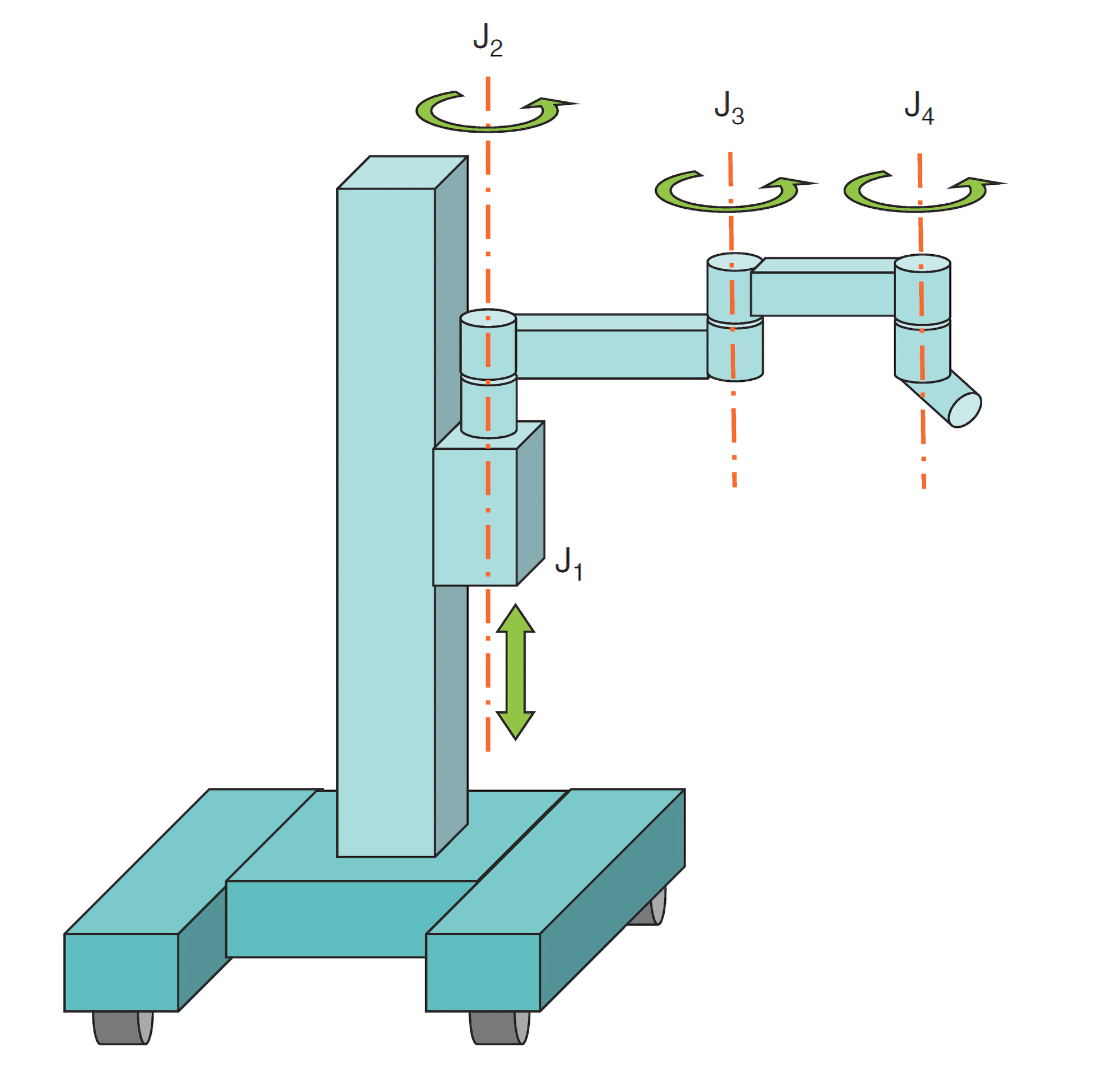
Призматический шарнир снабжен электродвигателем, в остальных трех есть только тормоза с кнопочной фиксацией. Около пациента постоянно находится ассистент хирурга, который перед операцией вручную выставляет манипуляторы в нужные позиции и по команде меняет инструменты, закрепленные на манипуляторах. Он получает команды по интеркому, соединяющему консоль хирурга и консоль пациента.
Кстати, если бы не встроенная голосовая связь, хрестоматийное «Скальпель!» пришлось бы буквально кричать. В кино в операционной стоит напряженная тишина, но реальный уровень шума там около 45 дБ, а во время распаковки хирургических инструментов он достигает 75 дБ. Будто рядом с врачами работает пылесос или кухонная вытяжка.
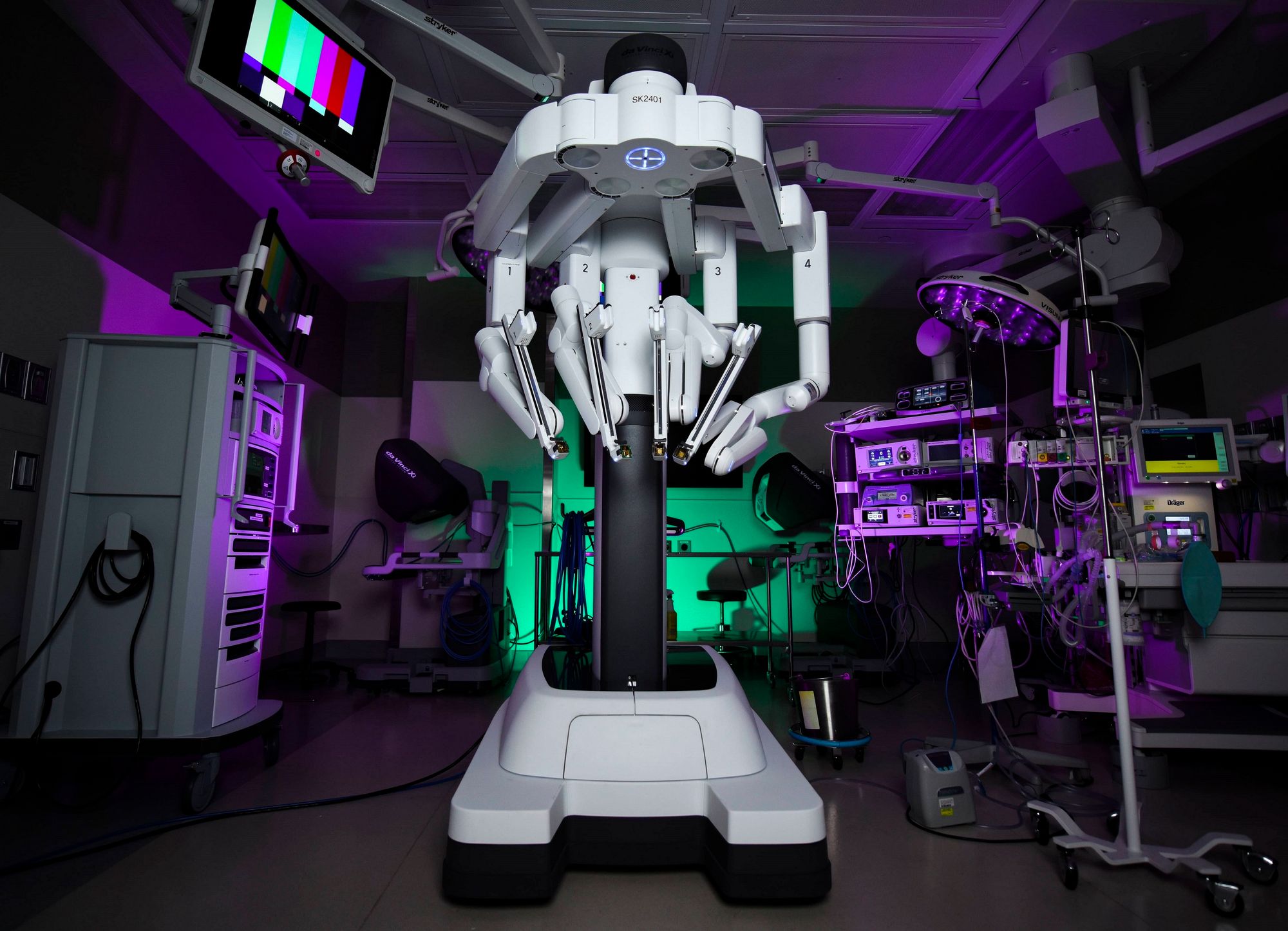
da Vinci Xi устроен сложнее. У этой версии робота пассивные манипуляторы выдвигаются на стреле над операционным столом и закреплены на балке, которая вращается на 360 градусов. Благодаря такой конструкции, хирурги не ограничены в выборе точек входа в организм пациента.
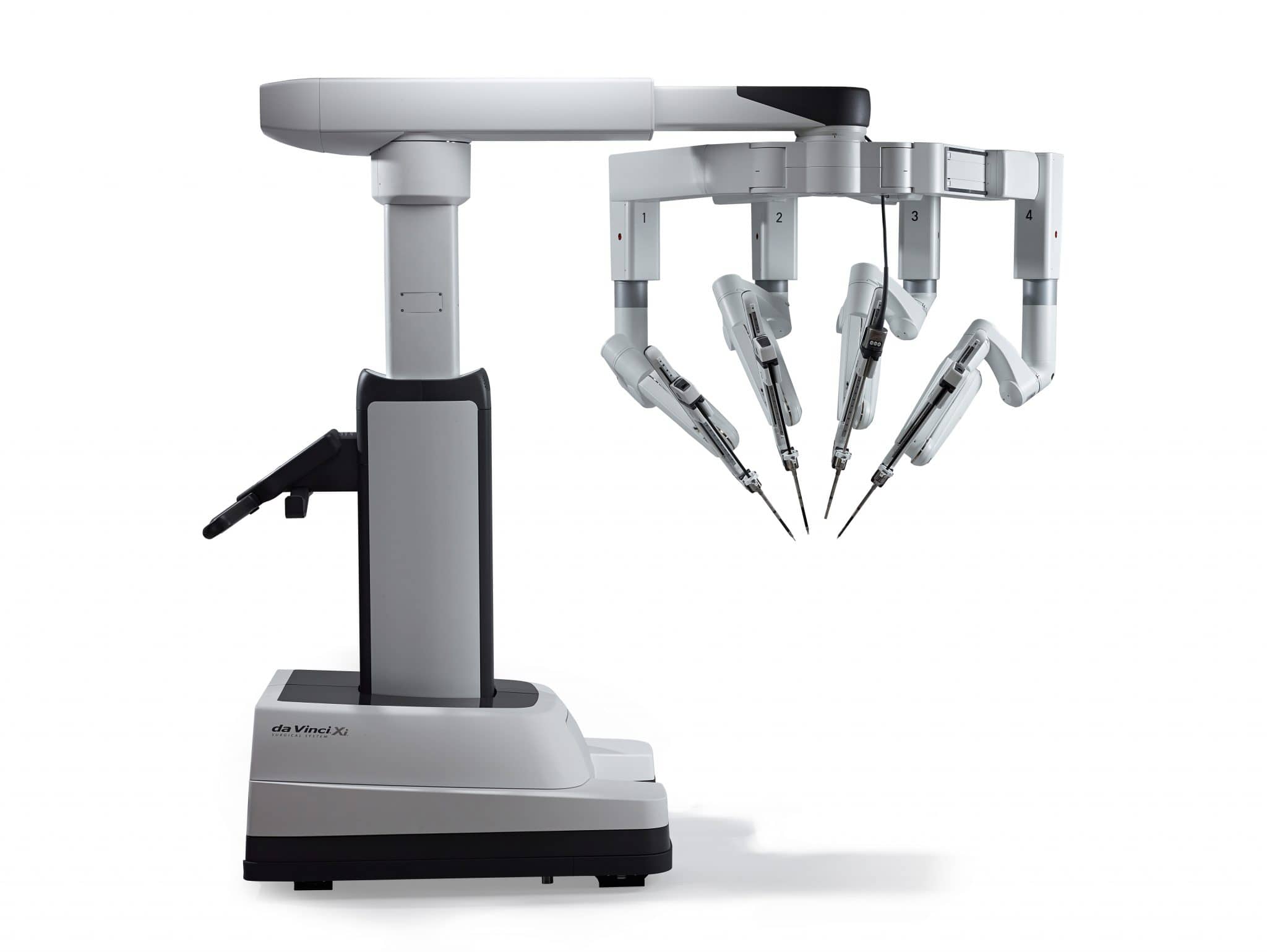
К тому же, пассивные манипуляторы da Vinci Xi не такие уж и пассивные. В их суставы встроены электрические приводы. Ассистент хирурга выбирает нужный тип операции на сенсорном экране консоли. Затем он пододвигает робота в нужное место, ориентируясь на перекрестье лазерного прицела, которое проецируется на пациента, и da Vinci сам занимает оптимальное положение для стыковки с троакарами.
А еще da Vinci можно синхронизировать с автоматизированным операционным столом. Он позволяет наклонять пациента прямо во время операции, так, чтобы сила притяжения облегчила доступ к определенным органам.
Активные манипуляторы
Все, что находится ниже четвертого сустава da Vinci, контролирует непосредственно хирург.
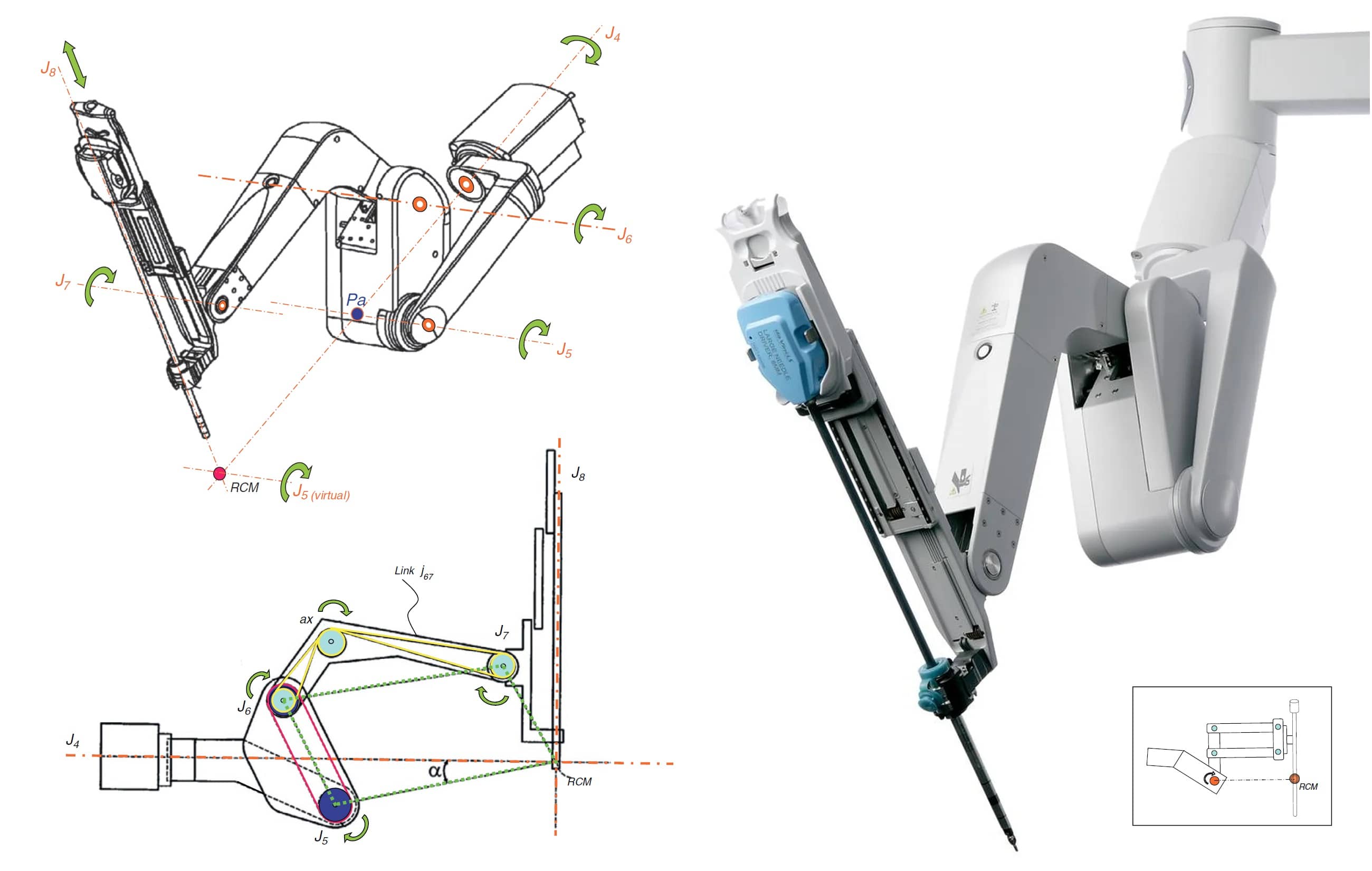
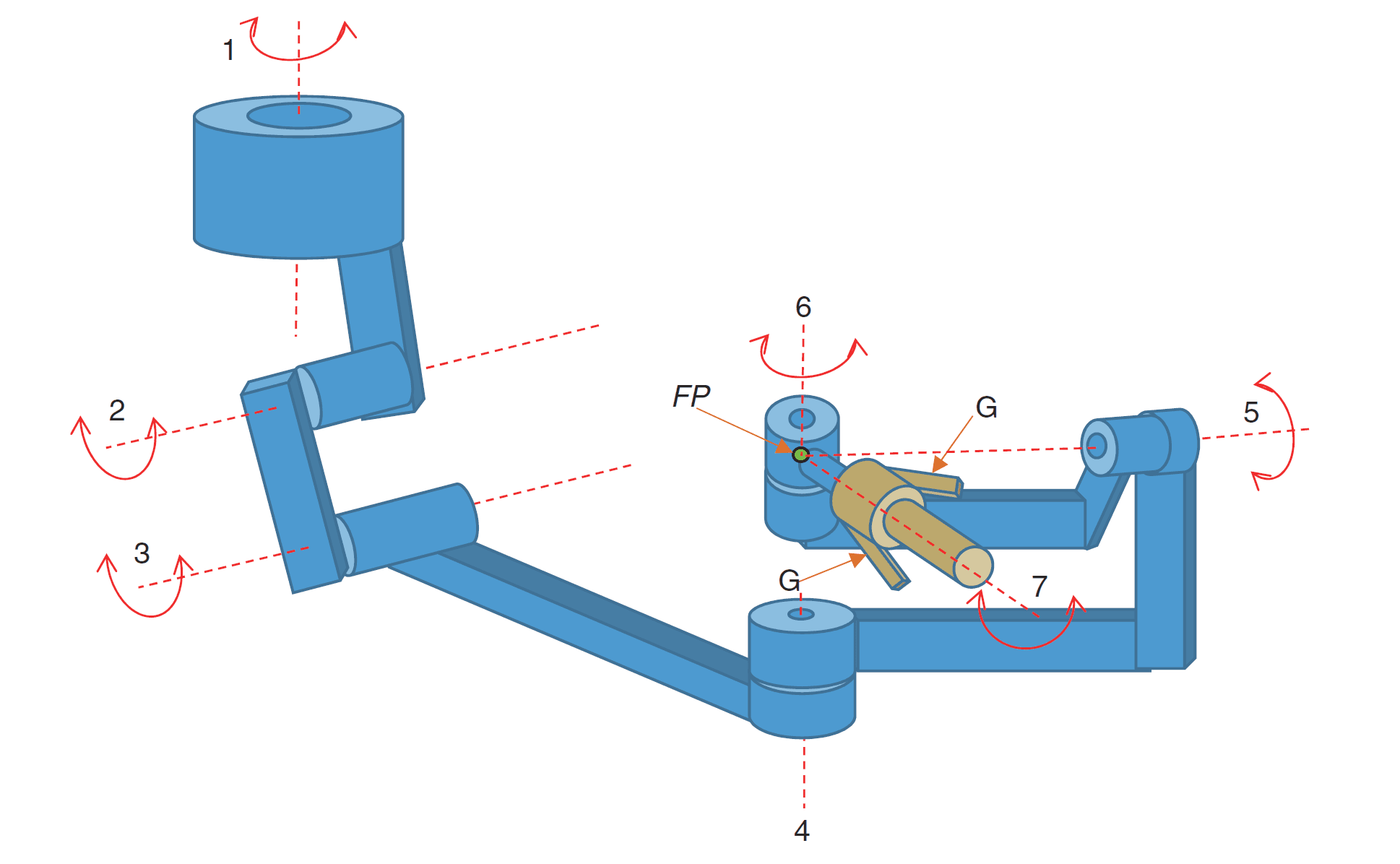
В основе активных манипуляторов RCM-механизм, напоминающий параллелограмм. Это сокращение расшифровывается, как Remote Centre of Motion, удаленный центр движения.

Проще говоря, манипуляторы сконструированы так, чтобы все их движения проходили через одну неподвижную точку — то место, где они вводятся в организм. Как бы хирург ни наклонял манипуляторы, они не давят на ткани в месте разреза и не травмируют пациента.
Как говорится, лучше один раз увидеть.

Тут-то и пригодились наработки Мадхани. В Black Falcon приводы были расположены у основания манипулятора. Усилие передавалось при помощи системы боуденовских тросов. Таких же, как в велосипедных тормозах и автомобильных спидометрах.
Использовав по паре тросов в полимерной рубашке на каждый сустав, инженеры Intuitive Surgical убрали из активной части манипуляторов электродвигатели. Это сделало руки робота легче и, главное, компактнее.
Инструменты EndoWrist

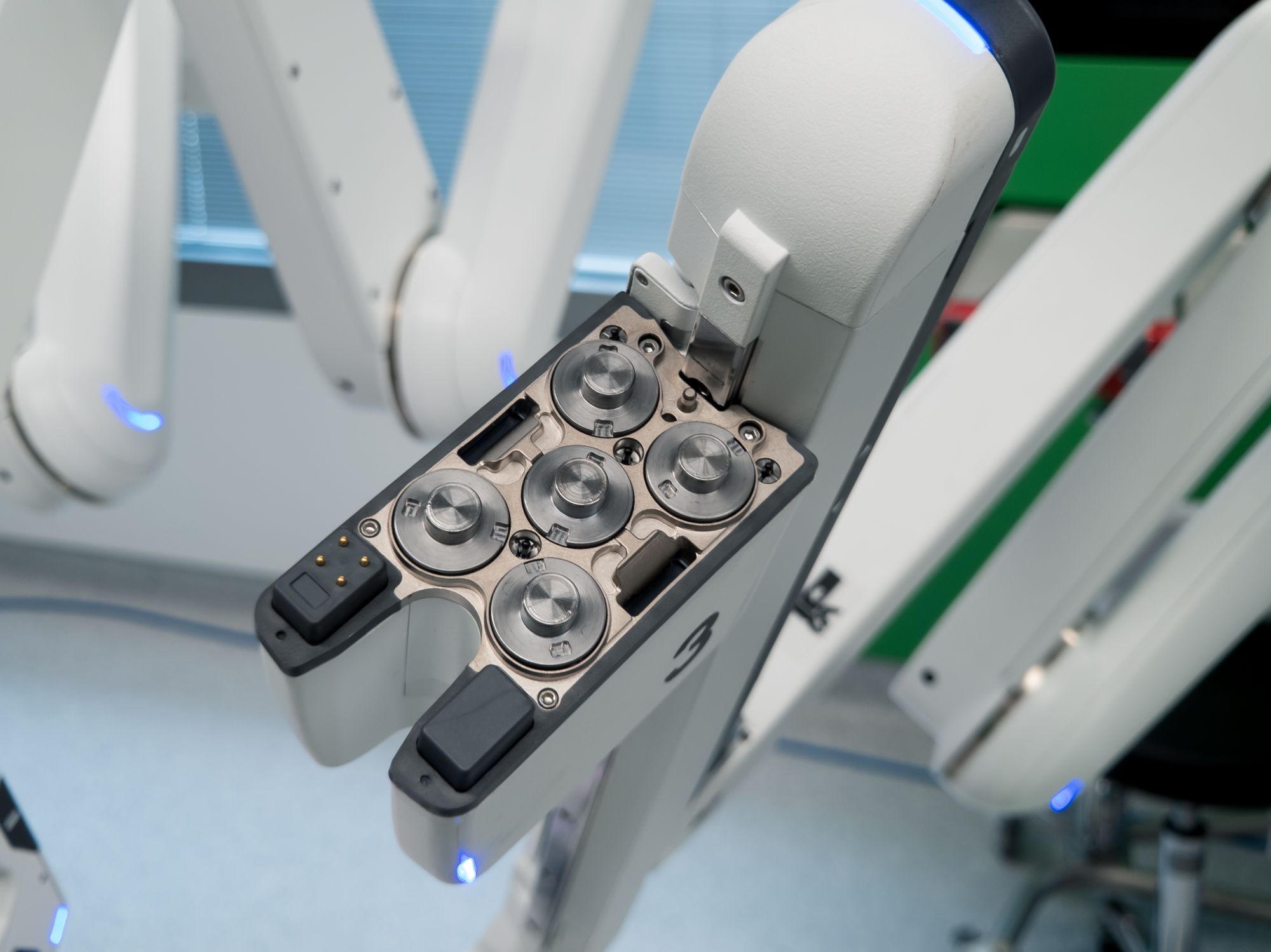
На конце активных манипуляторов расположена площадка с вращающимися коннекторами — крепление для сменных хирургических инструментов под названием EndoWrist. С ними связано больше 200 патентов — это, пожалуй, самая изобретательная часть конструкции da Vinci.

Первоначально, инструменты напоминали мечехвоста: плоский «блок управления» с системой натяжения тросов, хвостовой вал диаметром 8,5 мм и длиной до 38 см и жало — наконечник, выполненный максимально похоже на один из традиционных хирургических инструментов: ножниц, щипцов, иглодержателей, ретракторов, степлеров, коагуляторов.

Взять, например, щипцы — наиболее ходовой инструмент в малоинвазивной хирургии и, в то же время, сложнейший в части механики.
Щипцы EndoWrist состоят из карданных шарниров, каждый из которых приводится в движение тросами, действующими наподобие сухожилий. Такая конструкция обеспечивает 7 степеней свободы, как у человеческого запястья, и даже больший диапазон движений.

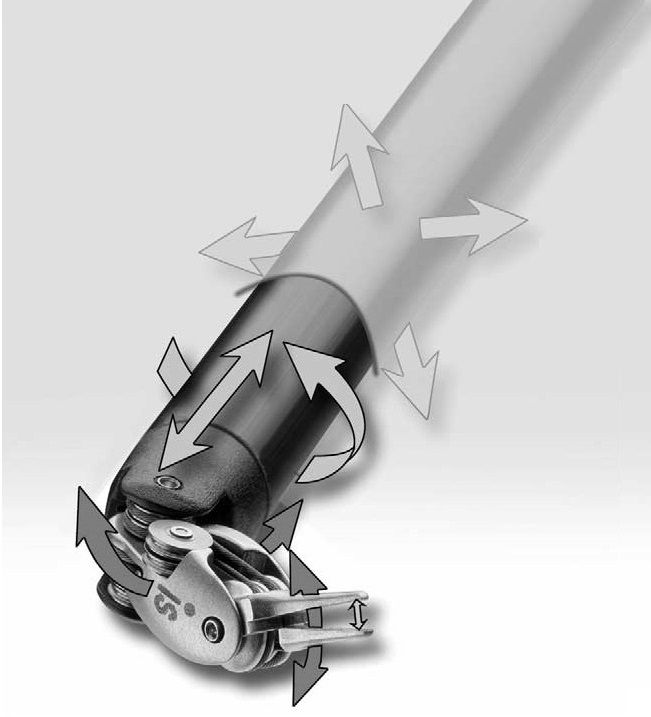
Со временем инженеры нашли способ уменьшить диаметр вала до 5 мм, и реализовали щипцы с более сложной конструкцией из четырех последовательных шарниров.
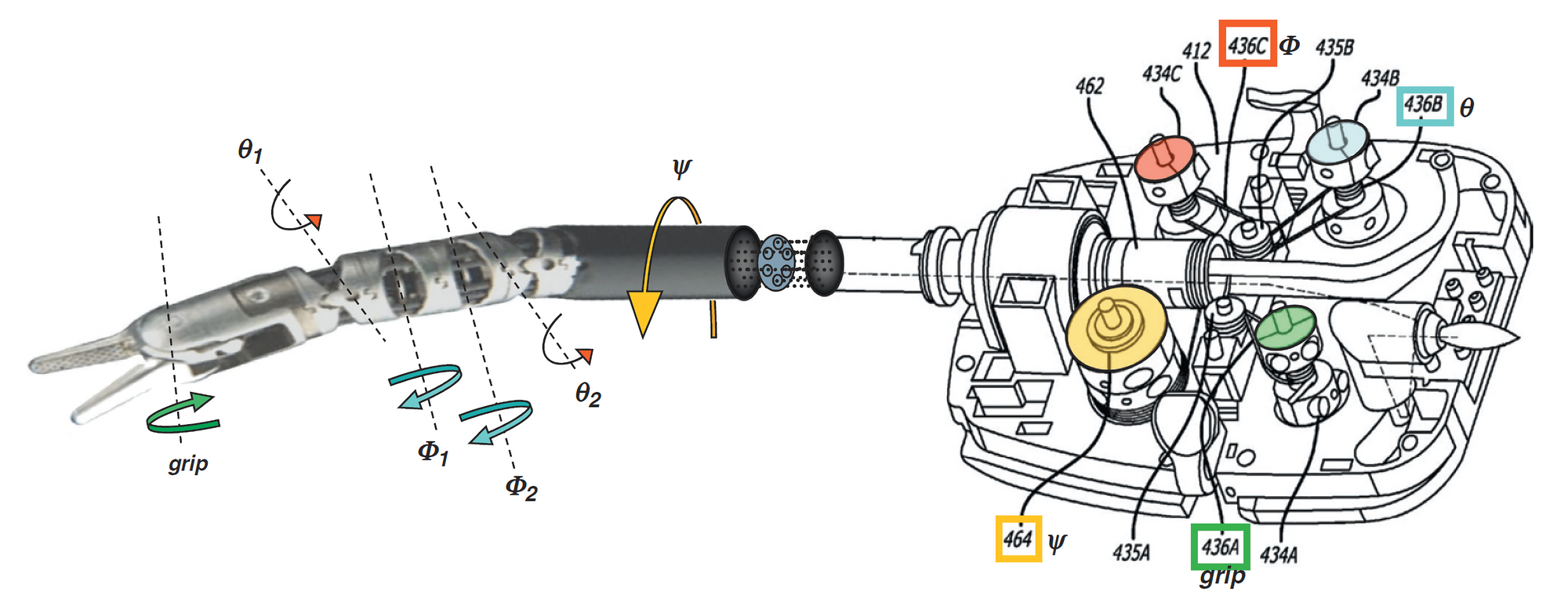
Увы, хирургические инструменты приходится стерилизовать после каждой операции, поэтому EndoWrist служат недолго. В зависимости от типа инструмента, они выдерживают от 5 до 10 попаданий в автоклав. Если продолжать стерилизовать инструмент, тросики теряют прочность и рвутся.
К концу 2021 года Intuitive Surgical обещает выпустить на европейский рынок инструменты с увеличенным ресурсом — от 12 до 18 применений.
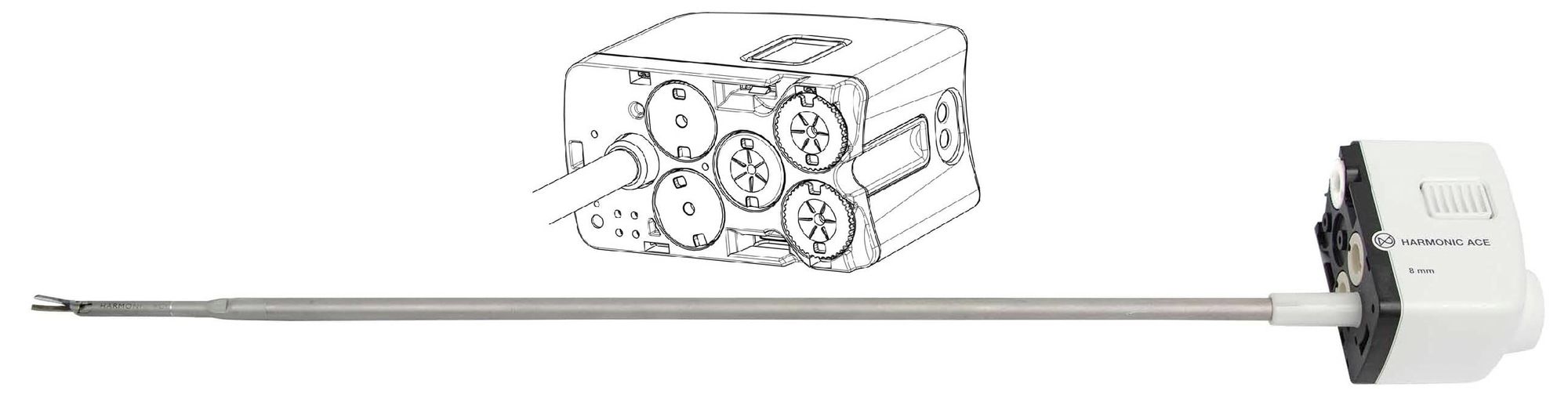
За количеством использований следит датчик на базе терморезистора. Робот отслеживает оставшийся ресурс и перестает работать с инструментом, когда счетчик доходит до нуля.
3D-эндоскоп

Глазами хирургу служит трехмерная камера, собранная из пары эндоскопов конструкции Хопкинса, упакованных в одну трубку. Объективы разнесены всего на 6 мм друг от друга, но этого хватает, чтобы создать стереоскопическую картинку. Между ними протянут оптоволоконный кабель, который дает свет и, нагреваясь, не дает линзам запотевать.
За объективами скрываются «трехчиповые» камеры, в которых за регистрацию красного, зеленого и синего цветов отвечают отдельные матрицы. Похожее решение используют в камерах космических аппаратов, оно позволяет улучшить цветопередачу.

Первоначально эндоскоп da Vinci имел диаметр 12 мм, угол обзора: 60°, разрешение 1280 x 720 и устанавливался на специально предназначенный для него манипулятор. Новые 8 мм эндоскопы имеют разрешение 1280 x 1024 и угол обзора до 80°. У них универсальное крепление, которое подходит ко всем 4 манипуляторам робота. К тому же, их можно использовать «с рук», во время подготовки к роботизированной операции.


Современные эндоскопы da Vinci оснащены инфракрасной подсветкой. Она нужна, чтобы подсвечивать различные вещества-маркеры. Их вводят пациенту перед операцией, а затем дожидаются, пока маркер осядет в определенных видах тканей.
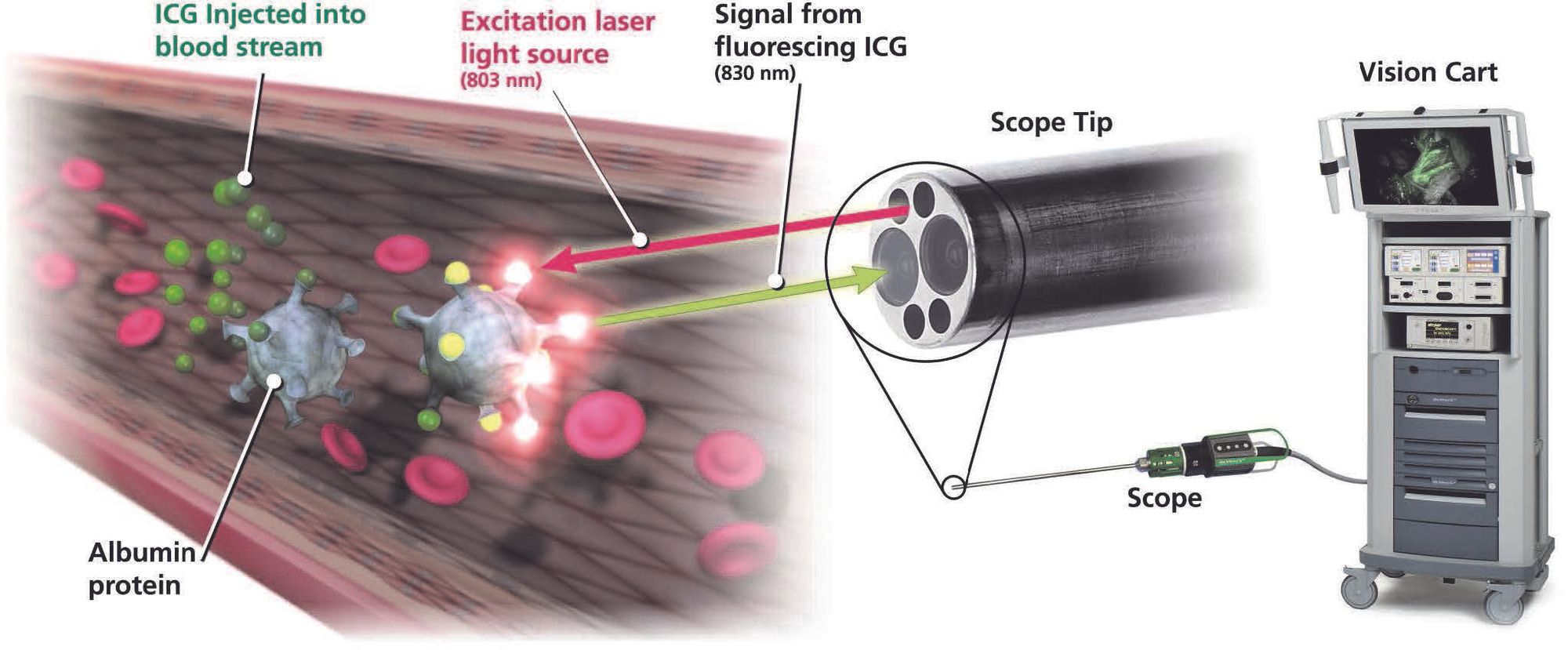
Например, индоцианин зеленый (ICG) быстро связывается с белками плазмы крови и распространяется с ними по организму. В инфракрасном свете он делает видимыми даже мелкие сосуды.
Видеостойка
Последний компонент da Vinci — тележка с массой вспомогательного оборудования, от ящиков для инструментов и баллонов с азотом, до электрохирургического генератора. Там же находится источник света для эндоскопа — яркая ксеноновая лампа. Но главное в этой стойке — ядро — блок с центральным компьютером, который отвечает за движения робота.
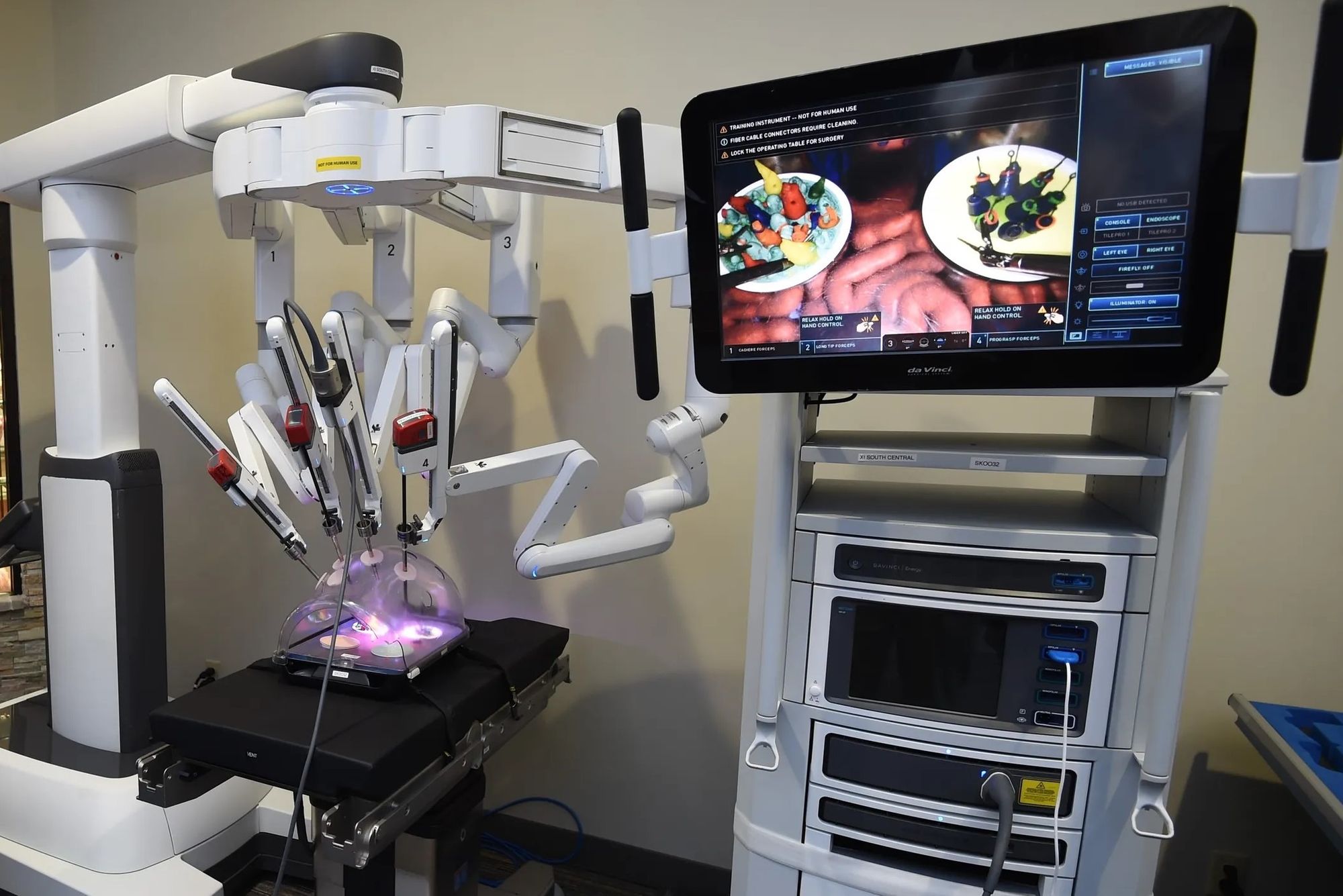
Сравнительно старый da Vinci S 2006 года выпуска располагал 48 энкодерами и 96 аналоговыми входами. Данные с них считывались сетью из 24 микроконтроллеров и целочисленных сигнальных процессоров (DSP), работающих параллельно.
Их общая пиковая производительность достигала 384 мегафлопс, а средняя — 190 мегафлопс. Не так уж много. Для сравнения, пиковой производительностью в 200 мегафлопс щеголял Pentium 200 еще в 1996 году. Но то микроконтроллеры. Характеристики центрального компьютера своего робота-хирурга Intuitive Surgical не раскрывает до сих пор.

Даже на конференции для инвесторов в 2017 году CEO компании Гарри Гутхард рассказал совсем немного. Он обмолвился, что вычислительная мощность центрального компьютера последних версий da Vinci равняется 7 ноутбукам, а 50 распределенных по системе контроллеров сравнимы с iPhone. Кроме того, робот снабжен сотней датчиков и набором аппаратных сторожевых таймеров, которые отвечают за самодиагностику и обнаружение неисправностей в режиме реального времени.
Консоли хирурга и пациента соединяются по оптоволокну через сеть TCP/IP. Защиту от потери пакетов обеспечивает CRC-алгоритм. Последние версии da Vinci снабжены Wi-Fi-модулем. Он нужен, чтобы стримить на Twitch устраивать онлайн-трансляции операций, отсылать телеметрию и обновлять прошивку «по воздуху», как в каком-нибудь смартфоне.
da Vinci Xi поддерживает беспроводной стандарт IEEE 802.11, на частоте 2,4 ГГц в промышленном, научном и медицинском (ISM) диапазоне. Данные шифруются по стандарту AES
Что касается программного обеспечения, da Vinci работает на Linux, модифицированном для работы в реальном времени. Возможно, это некое развитие проекта RTLinux.
Intuitive Surgical раздает списанных роботов исследователям, но ядро не входит в комплект da Vinci Research Kit. Роботы из этой программы работают под управлением обыкновенной Ubuntu. Для них существует отдельная прошивка с открытым исходным кодом.
Недостатки da Vinci
За 22 года клинической практики da Vinci приобрел репутацию продуманной и безопасной машины, но этот робот далеко не идеален. При его создании инженерам пришлось пойти на множество компромиссов.
Низкая точность
Манипуляторы da Vinci не получились такими изящными, если бы внутри находились обычные электрические приводы. Вместо них использовали тросы, но у этого подхода много недостатков.

Движения манипуляторов сложно контролировать, ведь датчики находятся со стороны двигателей, которые «дергают за ниточки». Еще пара проблем — люфты и потери усилия. При каждом движении робота тросы смещаются и трутся о полимерную оболочку. И чем меньше радиус кривизны троса, тем сильнее трение. Это трудно компенсировать программно, особенно если пытаешься сохранить плавность движений.
Поэтому da Vinci плохой кандидат на роль автономного робота-хирурга. После видео с виноградинкой звучит неправдоподобно, но точность механики робота — примерно 2 мм, а погрешность при многократном возвращении инструмента в одну и ту же точку и того хуже — около 1 см. Это незаметно, потому что инструменты контролирует хирург, который постоянно корректирует движения.
Рабочий объем и неравномерность усилий
Необходимо учитывать, что точность, как и сила робота, — величина непостоянная. Они зависят не только от числа сочленений и подвижности шарниров, но и от положения манипуляторов в пространстве.
В одной точке робот может приложить большее усилие, чем в другой. То же верно и для точности позиционирования. В одних точках погрешность больше, чем в других.
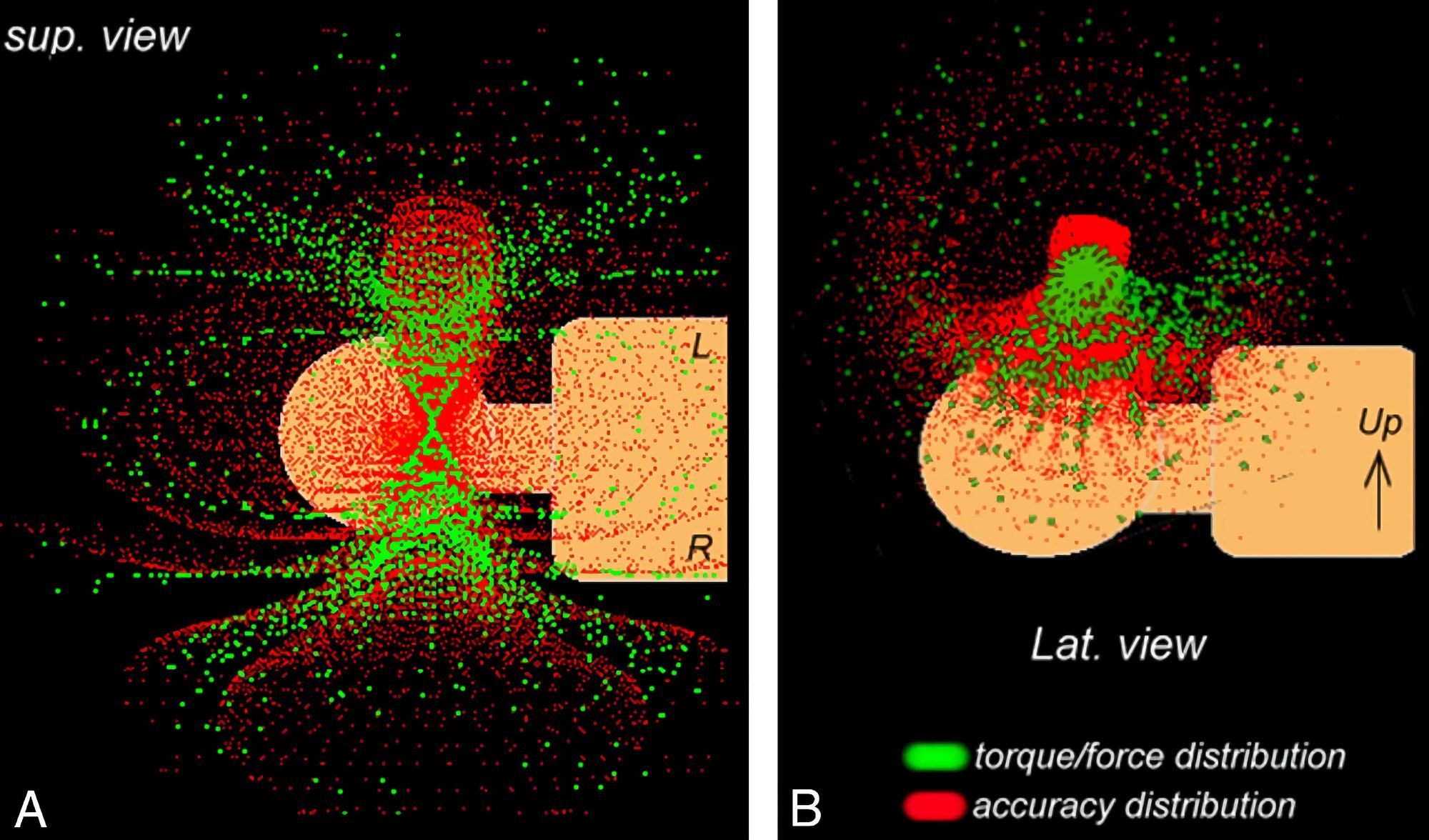
Поэтому полезный хирургический рабочий объем, меньше того, что можно было бы предсказать по размеру манипуляторов. Например, da Vinci Si может работать в полости не менее 125 см³. К тому же, некоторые координаты в рабочей области могут быть недоступны из-за того, как рассчитывается движение.
Ограниченная обратная связь
Еще один значимый минус заключается в том, манипуляторы робота не дают тактильной обратной связи. Во время обычной открытой операции хирург во многом полагается на осязание, например, чтобы отличить один вид тканей от другого или аккуратно затянуть шов. da Vinci лишает хирурга этого чувства. Этот недостаток отмечают, пожалуй все, кто критикует эту систему.

Хотя наиболее опытные хирурги говорят, что чувствуют легкий контакт с некоторыми мягкими тканями, по большому счету, все, что можно ощутить управляя da Vinci, это столкновение инструментов. В ответ на критику в Intuitive Surgical Inc. говорят, что больше доверяют зрению, чем осязанию.
Проблема в том, что хирургические инструменты переживают неоднократную стерилизацию в автоклаве. Датчикам давления, как и любым другим сенсорам, которые можно было бы расположить на кончиках инструментов, необходимо выдерживать воздействие пара, разогретого до 130 С при давлении 2 атм. А еще, желательно, чтобы после этого они не требовали калибровки. Подходящие сенсоры сделают сменные инструменты значительно дороже и все равно отправятся на выброс после десятка использований.
Продолжительность операций
Исследования показывают, что операции с использованием роботов в среднем быстрее открытых, но дольше обычных лапароскопических. А с ростом продолжительности растут риски — пациент дольше находится под общим наркозом и в ткани всасывается больше углекислого газа.
Цена
Наконец, нельзя забывать о деньгах. Современные роботы-хирурги Intuitive Surgical стоят около 2 млн долларов за штуку, но их продажи приносят компании только чуть больше 30% процентов прибыли. Остальное приходится на техническое обслуживание и поставки инструментов.

Расходники очень дорого стоят. По цене одних щипцов EndoWrist можно купить несколько традиционных лапароскопических инструментов, рассчитанных на сотни операций. И даже не на Aliexpress (оказывается, там продаются и такие штуки). Чтобы выйти в ноль после покупки робота da Vinci, необходимо проводить от 150 до 300 роботизированных операций ежегодно в течение шести лет.
Роботизированная операция в США стоит на 3–6 тыс долларов дороже обычной лапароскопической
Поэтому руководство больниц не заинтересовано в том, чтобы робот простаивал. В США пациентов нередко «подталкивают» к роботизированным операциям, хотя обычные дешевле и могут быть лучше с медицинской точки зрения.
В чем сложность разработки роботов-хирургов
В числе минусов da Vinci могло бы оказаться и низкое разрешение визора. На бумаге по разрешению он не дотягивает до современных VR-гарнитур, но в реальности картинка четкая и резкая, отдельные пиксели не заметны. Да и в научных публикациях качество изображения не критикуют.
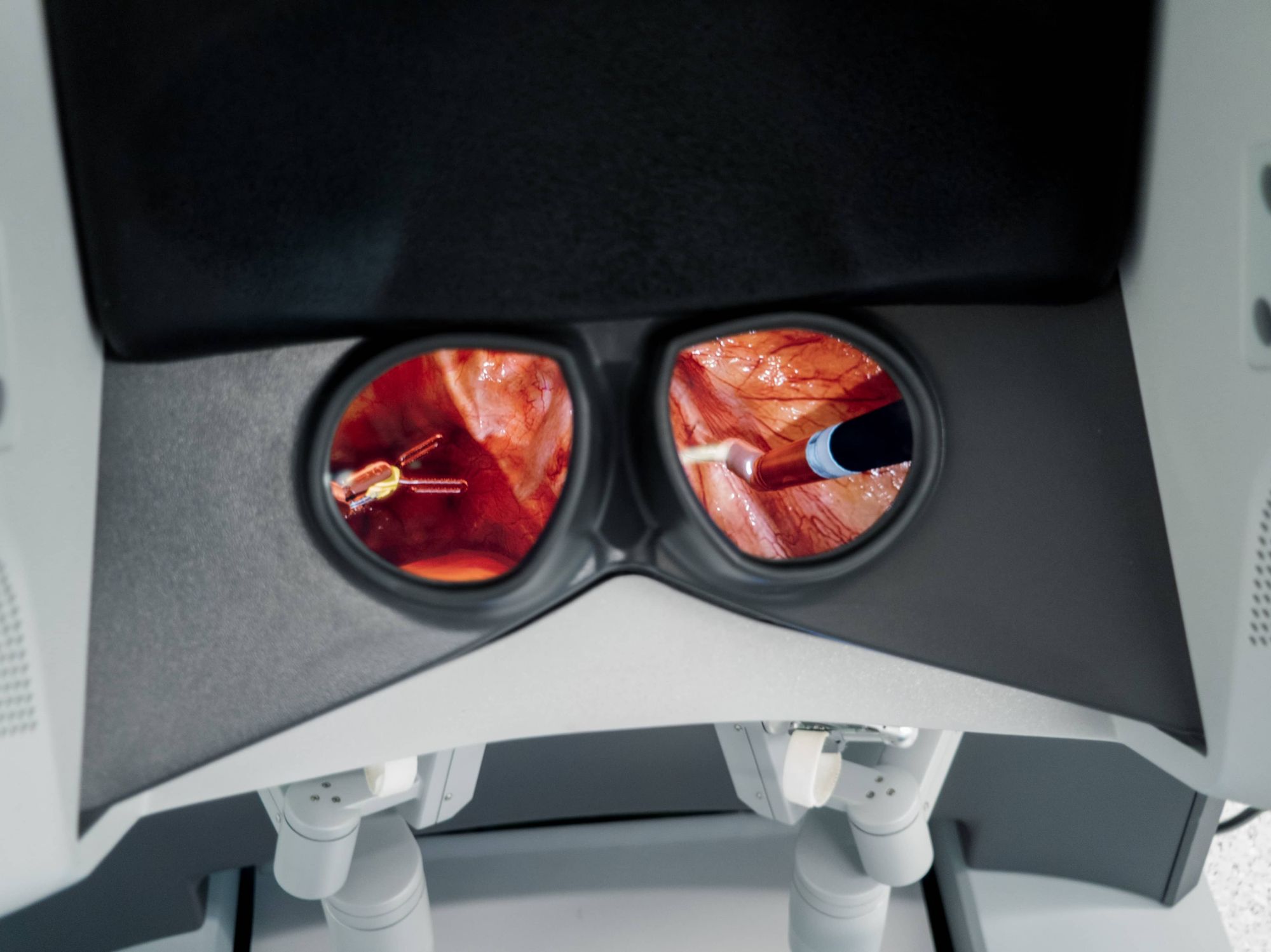
Конечно, все не так уж просто — вместе с визором нужно модернизировать и камеры лапароскопа. И все же, это хороший пример. Кажется, что при помощи распространенных технологий уже сейчас можно создать куда более совершенных роботов-хирургов, однако на рынке доминирует система, которая принципиально не менялась уже 20 лет.
Действие ключевых патентов Intuitive Surgical закончилось, так что дело не в юристах, которые душат конкурентов. Препятствия лежат в другой плоскости.
Просто очень сложная инженерная задача
Идеальный хирургический робот должен быть точным, ловким, быстрым, способным совершать тонкие движения и прикладывать большую силу, надежно захватывать и поднимать грузы. Беда в том, что необходимые характеристики сложно взаимосвязаны, и добиться всего и сразу — головоломная задача.

Возьмем точность робота. Она зависит от разных факторов. Вот неполный список: конструкция и масса манипулятора, зазоры и люфты, натяжение тросов, трение, разрешение датчиков, погрешности в вычислениях, качество деталей и даже температура в операционной. И все эти факторы взаимодействуют друг с другом.
Например, люфты и зазоры. Точность требует минимального зазора между подвижными частями робота, но сокращение зазоров увеличивает трение в шарнирах.
Высокое трение увеличивает усилие, необходимое для перемещения, и вводит нелинейные параметры в уравнения движения, а это затрудняет управление манипулятором. Проблема усугубляется, если соединения длинные, а грузоподъемность высокая, так как в таких конструкциях трение еще сильнее.
Другой пример — жесткость конструкции. Она повышает точность, но увеличивает размер и массу манипулятора. Из-за этого возрастает инерция, робот движется медленнее и отстает от движений хирурга.
Робота очень сложно сделать хорошим во всем без исключения, а может быть и вовсе невозможно. Инженерам приходится лавировать между противоположными требованиями, и это неизбежно приводит к компромиссам.
Сложная среда без жестких рамок
Условия, в которых работает робот-хирург, не дают сделать его действительно автономным. Нейрохирургические роботы и системы вроде ROBODOC используют жесткую привязку к координатной сетке. Для них за точку отсчета берутся определенные участки костей, но для полостных операций этот метод не походит.
Внутри живого организма все деформируется, меняет форму и влажно блестит в свете эндоскопа. Там не на что ориентироваться. Не говоря уже о том, что камера пачкается и, порой, запотевает, несмотря на встроенный обогрев.
Сложность программирования
Программирование робота-хирурга также непростая задача. За видимой легкостью, с которой движения человека передаются роботу, стоят сложные расчеты. Отправной точкой для них становятся показания датчиков поворота, энкодеров в шарнирах контроллера.
Чтобы преобразовать показания энкодеров в координаты используется прямая кинематика. Чтобы привести манипулятор в полученные координаты, проводят обратную операцию, рассчитывают углы поворота суставов манипулятора при помощи инверсной кинематики. Она позволяет вычислить, при каких значениях углов должны быть установлены приводы для того, чтобы робот занял нужную позицию.

Обе задачи сводятся к решению систем алгебраических уравнений. Чем больше степеней свободы имеет робот, тем сложнее они становятся, особенно если движениями управляет 39 приводов, как у da Vinci S.
Зачастую приходится обходиться не точными, а приближенными решениями, найденными при помощи итерации. Вот только этот математический прием не дает никаких гарантий. Не факт, что с его помощью удастся вычислить решение, чтобы придать роботу нужную позу.
Вдобавок приходится рассчитывать для каждого привода скорость, пропорциональную углу перемещения, чтобы манипулятор не вышел за пределы безопасной траектории и не навредил пациенту. Чтобы снизить колебания инструментов, реализуют плавное ускорение и замедление. А еще стоит убедиться, что случайное деление на ноль или вычисление тангенса 90° однажды не повесит всю систему.
Безопасность и законодательство
Единственный сбой в работе робота-хирурга может стоить человеку жизни и похоронить весь проект. Так что общепринятое золотое правило здесь — чем проще конструкция, тем лучше. Инженеры сильно перестраховываются и редко используют перспективные, но непроверенные или незрелые технологии. И все равно, американскую FDA крайне нелегко убедить в безопасности системы.

Перед операциями на людях роботы-хирурги проходят бесчисленные проверки и испытания. Процесс затягивается на годы, и это делает разработку еще более сложной и дорогой. А если вы хотите продавать роботов где-то за пределами США, придется получать разрешения заново в каждой стране.
Во многом по этому до сих пор 71% выручки Intuitive Surgical приходится на штаты, и только 15% продаж на Европу и 10% — на страны Азии.
Сложность тестирования
И наконец, остается самая малость — доказать, что робот полезен с медицинской точки зрения. Никто не спорит с тем, что da Vinci облегчает работу хирургов, но не факт, что машина приносит пользу пациенту. Преимущества неочевидны и зачастую нет доказательств того, что для конкретного типа операций лучше использовать робота, а не обычные лапароскопические инструменты.
В докладе «Будущее хирургии» британский Королевский хирургический колледж отметил, что у нас недостаточно доказательств эффективности роботизированной хирургии, а продолжительные исследования таких процедур малополезны из-за частых изменений в конструкции роботов
И не удивительно. Это явно не тот случай, в котором можно без проблем организовать рандомизированное двойное слепое плацебо-контролируемое исследование. Тем более такое, за которое исследователей не распнет этическая комиссия. Как правило, приходится использовать менее надежные методы, а то и просто анализировать статистику по плановым операциям и опрашивать врачей.
Будущее роботов-хирургов
Информационные технологии приучили нас к регулярным, чуть ли не ежегодным революциям. В IT новая идея выстреливает, завоевывает популярность и устаревает за год. В медицине иначе. Из-за всех этих сложностей разработка и внедрение роботов-хирургов требуют колоссальных вложений, а инвестиции в эту сферу приносят результаты через десятки лет.
Но есть и хорошие новости — несмотря ни на что рынок хирургических роботов развивается (по прогнозам к 2025 году он вырастет на 13,14%). Растет конкуренция. Одна за другой на рынок выходят копии da Vinci. Например, корейский Revo-i и китайский Micro Hand S.
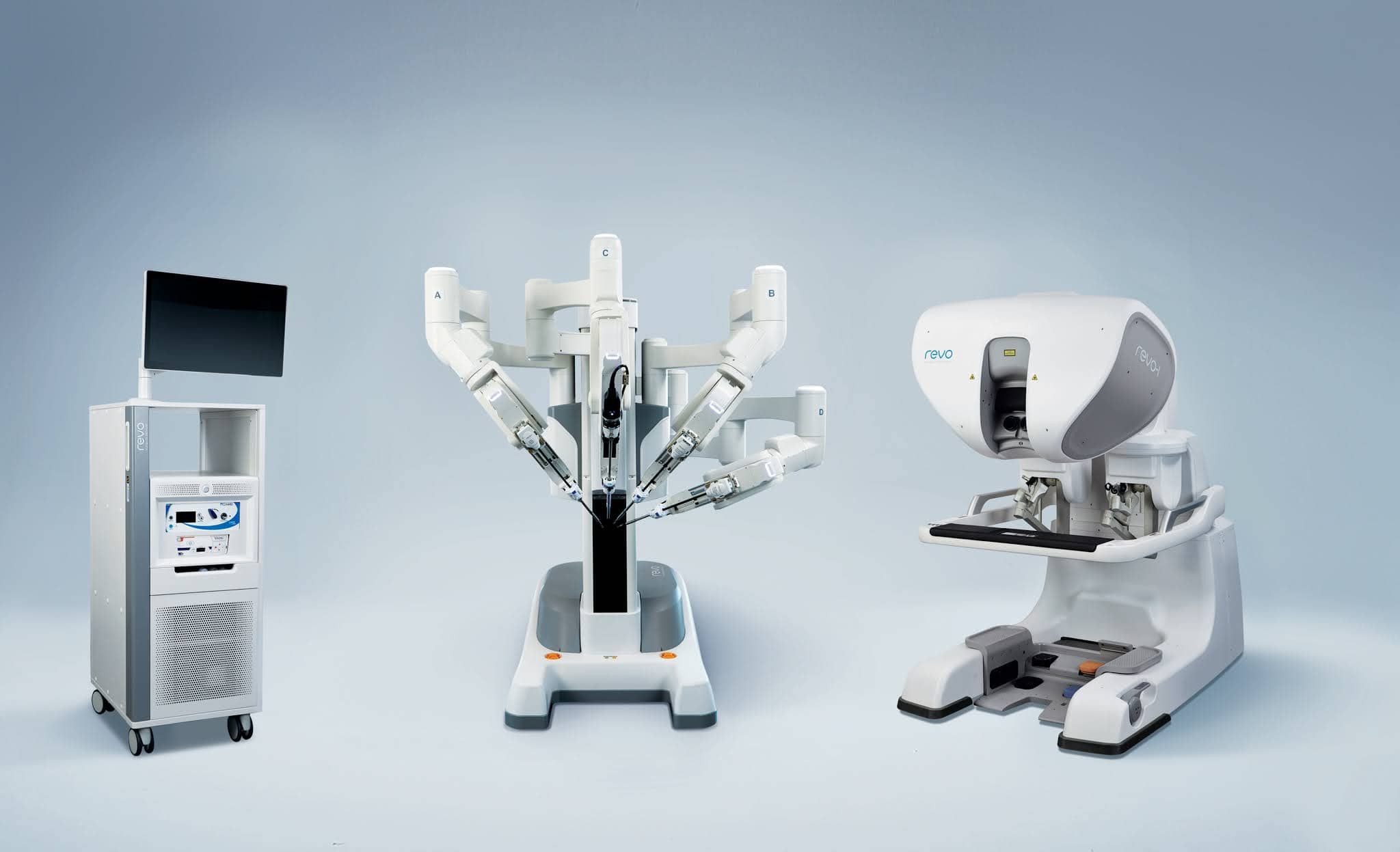
В то же время консервативность медицины оборачивается необычной возможностью — можно достаточно точно спрогнозировать развитие медицинской робототехники, взглянув на то, как инженеры комбинируют уже существующие технологии.
Гибкие манипуляторы
Прежде всего хирурги заинтересованы в большей гибкости манипуляторов. Это и большая свобода действий, и возможность проводить операции без видимых разрезов, через естественные отверстия в теле или перемещаясь к нужной точке в организме по крупным сосудам.
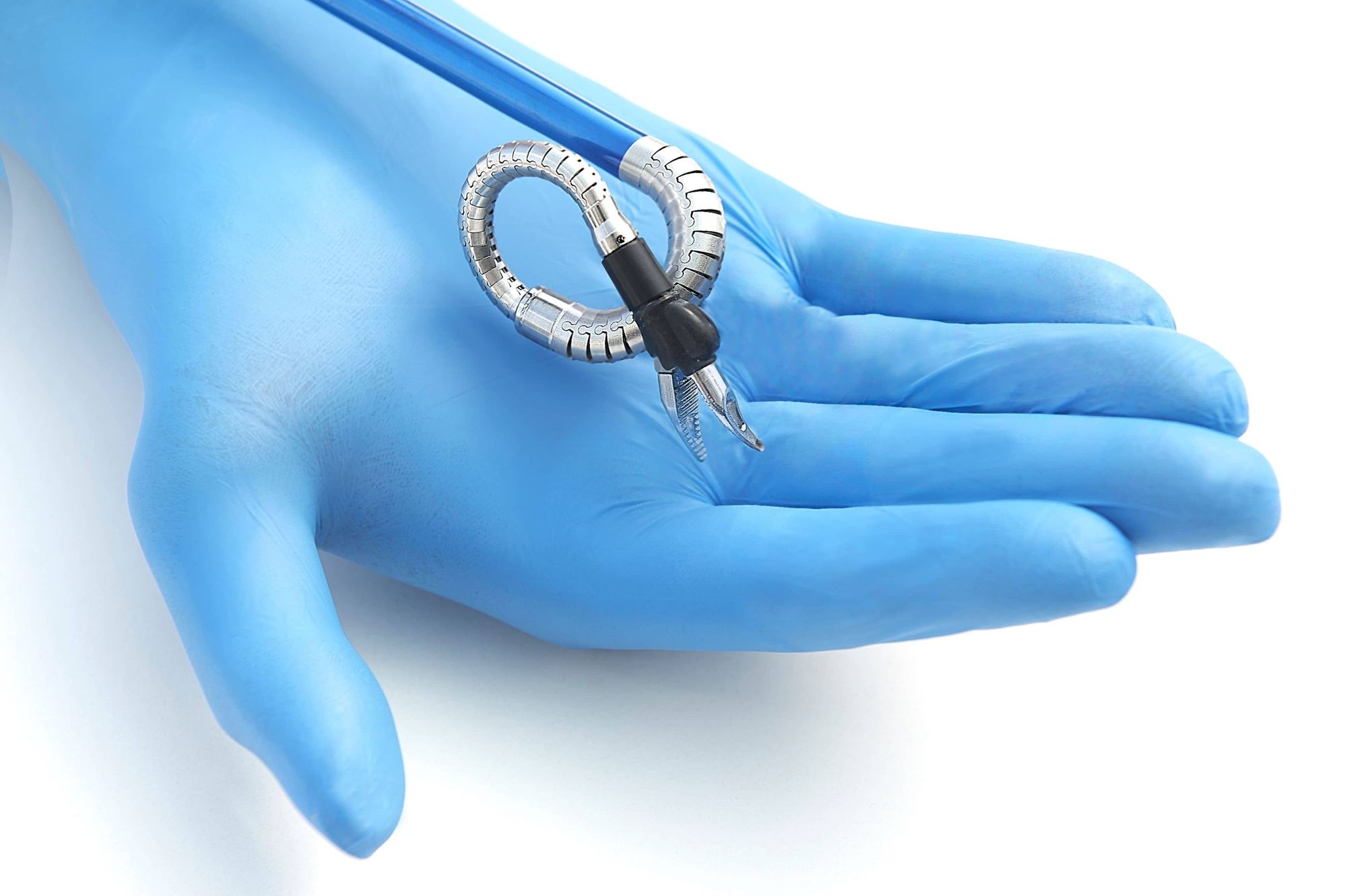
da Vinci SP уже может похвастаться многосуставными инструментами, которые вводятся в организм через единственное отверстие. Израильская система Hominis, которая недавно получила одобрение FDA, еще более гибкая. Инструменты этого робота хирурга гнутся на все 360 градусов, разве что в узлы не завязываются.
Существуют змееподобные роботы-эндоскопы, типа Flex и автоматизированные катетеры. Не так давно с помощью такого устройства провели серию операций на свиньях. Катетер добрался до сердечного клапана автоматически, следуя вдоль стенок сосудов и ориентируясь при помощи гибридного оптического датчика касания и алгоритмов машинного обучения.
Новые приводы
Параллельно идут эксперименты с новыми разновидностями двигателей на замену тросам и электрическим приводам. Исследуют все, вплоть до пневматики и гидравлики, но наиболее перспективными для малоинвазивной хирургии кажутся электроактивные полимеры — искусственные мышцы. Они не дороги, сильно деформируются, не занимают много места и развивают значительное усилие.
У микрохирургов другой фаворит — пьезоэлектрические приводы. Их мощность не зависит от массы ротора. Эти движки имеют такой высокий крутящий момент, что можно не ставить редуктор. Они компактны и мгновенно приходят в движение. Минимальный шаг пьезомоторов составляет тысячные доли угловой секунды. Это настолько мало, что их используют в конструкции сканирующих зондовых микроскопов для того, чтобы буквально ощупывать атомы. Вдобавок ко всему — их делают из керамики. Роботы на базе таких движков не мешают работе МРТ.
Одна беда — и тот и другой вариант требуют для работы высокого напряжения. Использовать несколько сотен вольт поблизости от пациента, страшновато, так что к этим разработкам относятся с крайней осторожностью.
Машинное обучение
В хирургию еще не внедрили блокчейн, но вот без машинного обучения не обошлось. Здесь оно способно принести пользу сразу на нескольких уровнях. Алгоритмы машинного обучения могут упростить расчет движений манипуляторов, а могут и автоматизировать целые этапы операции.
Так, в 2020 году команда Калифорнийского университета в Беркли при помощи видеозаписей натренировала сиамскую нейронную сеть накладывать вполне приличные ровные швы. Более того, еще в 2016 году во время реальной операции исследователи показали, что робот-хирург может самостоятельно сшить фрагменты кишки свиньи. Однако, тогда хирурги предварительно разметили область операции при помощи инфракрасных маркеров. На них робот и ориентировался во время работы. К сожалению, маркеры непрактичны — их непросто вживить и сложно удалить.
Основная проблема заключается в том, чтобы научить роботов использовать подобные навыки в изменчивых условиях человеческого организма.

Пока что алгоритмы учат полагаться на данные с камер. Так, исследователи из Беркли заставляют da Vinci самостоятельно выполнять базовые упражнения, предназначенные для начинающих хирургов — перемещать кольца с колышка на колышек на специальном стенде. Но то в лабораторных условиях. Пока что не ясно, сумеем ли мы натаскать алгоритмы машинного зрения для работы внутри организма. Однако, это не единственный путь.
Интеграция с медицинскими сканерами
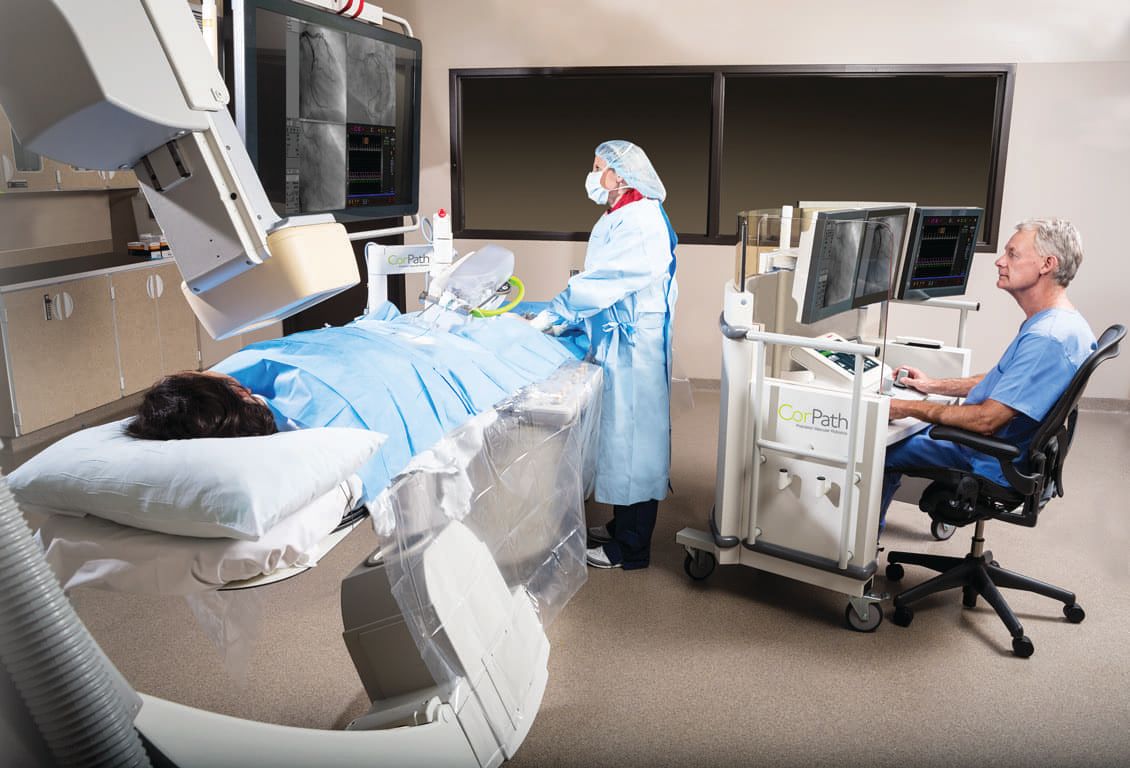
Святой Грааль медицинской робототехники — интеграция роботов с медицинскими сканерами: КТ, МРТ, УЗИ.
Существуют отдельные роботизированные УЗИ-системы и датчики, предназначенные для установки на da Vinci. Картинку с них обычно транслируют в отдельное окно в поле зрения хирурга. На компьютерную томографию полагаются кардиохирурги, использующие, роботизированные катетеры типа CorPath GRX и ортопеды, работающие с системами типа Loop-X.
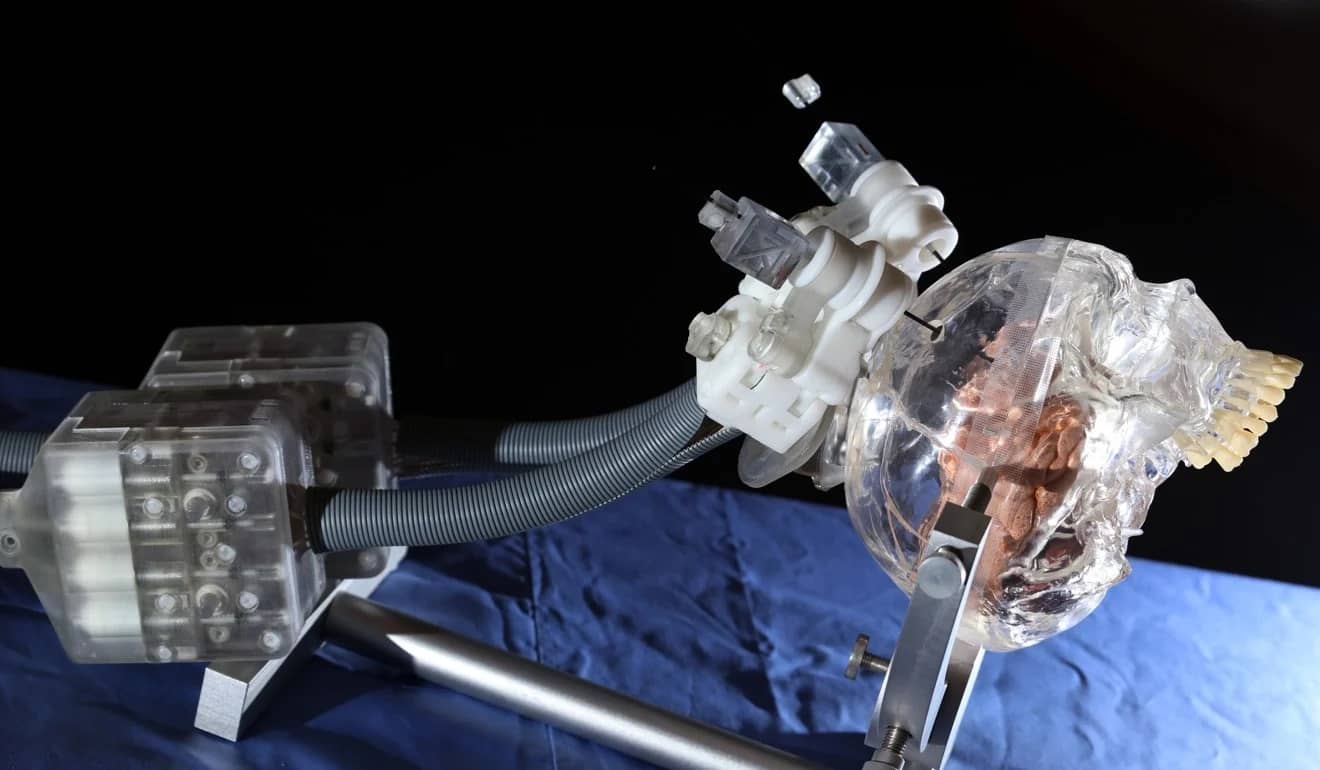
Добрались до испытаний хирургические манипуляторы, которые работают внутри включенного МРТ. Пока что это узкоспециализированные системы вроде робота для биопсии простаты на базе пьезоэлектрических приводов из Вустерского политехнического института (WPI).
Системы для общей хирургии, интегрированные с КТ и МРТ, существуют разве что на стадии концептов, но их потенциал можно представить, глядя на CyberKnife — медицинский ускоритель частиц, установленный на конце манипулятора KUKA KR 240.
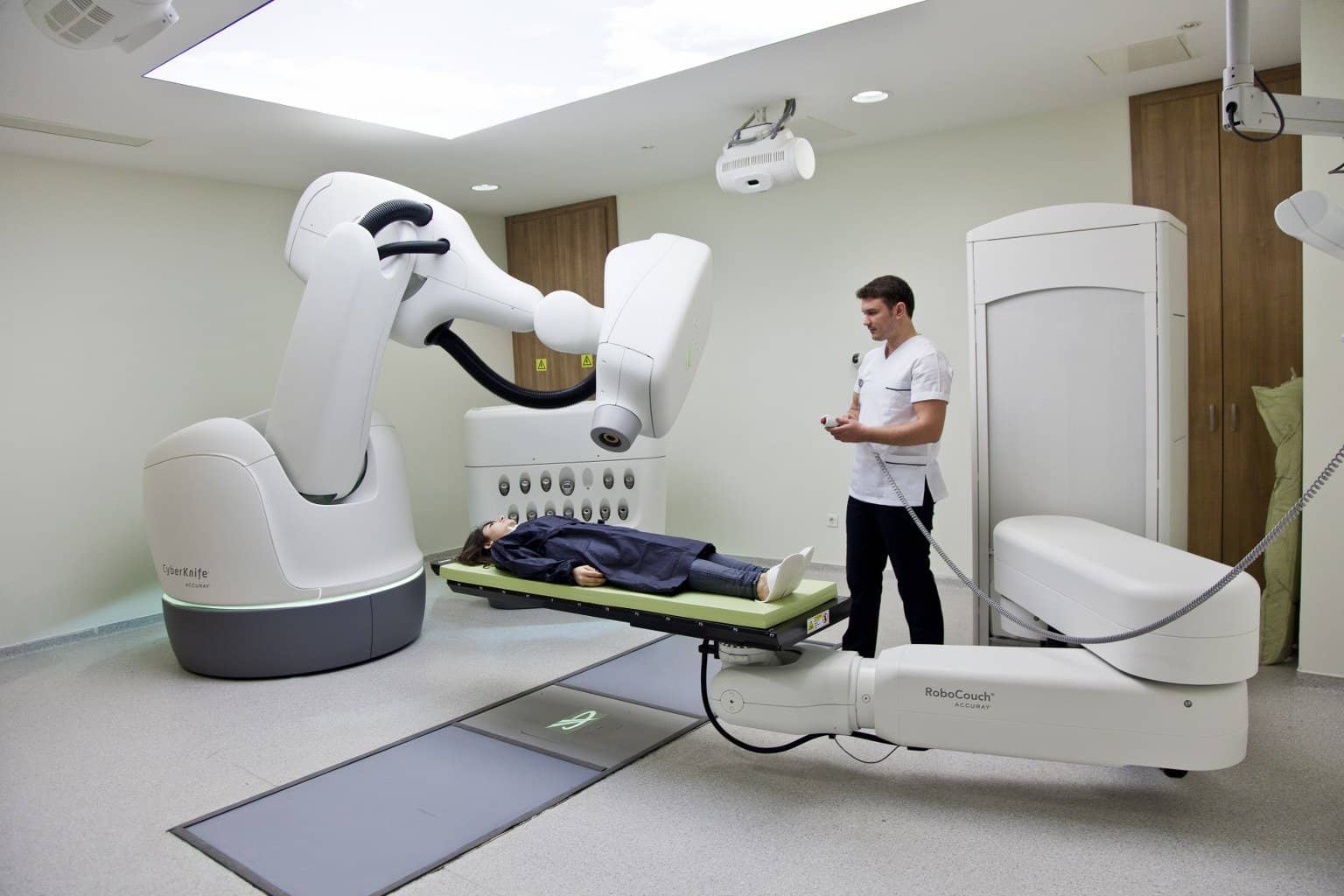
Этот робот создан, чтобы подсвечивать опухоли «живительным» рентгеном. Манипулятор делает это под разными углами, поэтому летальная доза излучения набирается лишь в четко очерченной области, даже если она расположена глубоко внутри организма.
CyberKnife регулирует интенсивность и диаметр потока частиц, подстраивает его под очертания опухоли. Для этого используется целый набор насадок. Самая сложная из них — MLC-диафрагма из 52 подвижных вольфрамовых пластин.

Все движения робота и мощность излучения рассчитываются заранее, на основе предоперационной компьютерной томографии опухоли. Врач выбирает из предложенных программой вариантов и утверждает план операции. Далее робот действует полностью автономно.
Чтобы добиться нужной точности, система контролирует положение опухоли в режиме реального времени. Для этого над операционным столом смонтирована пара рентгеновских трубок. Их лучи направлены на пациента под углом 45 градусов и подсвечивают зону размером около 15 см².
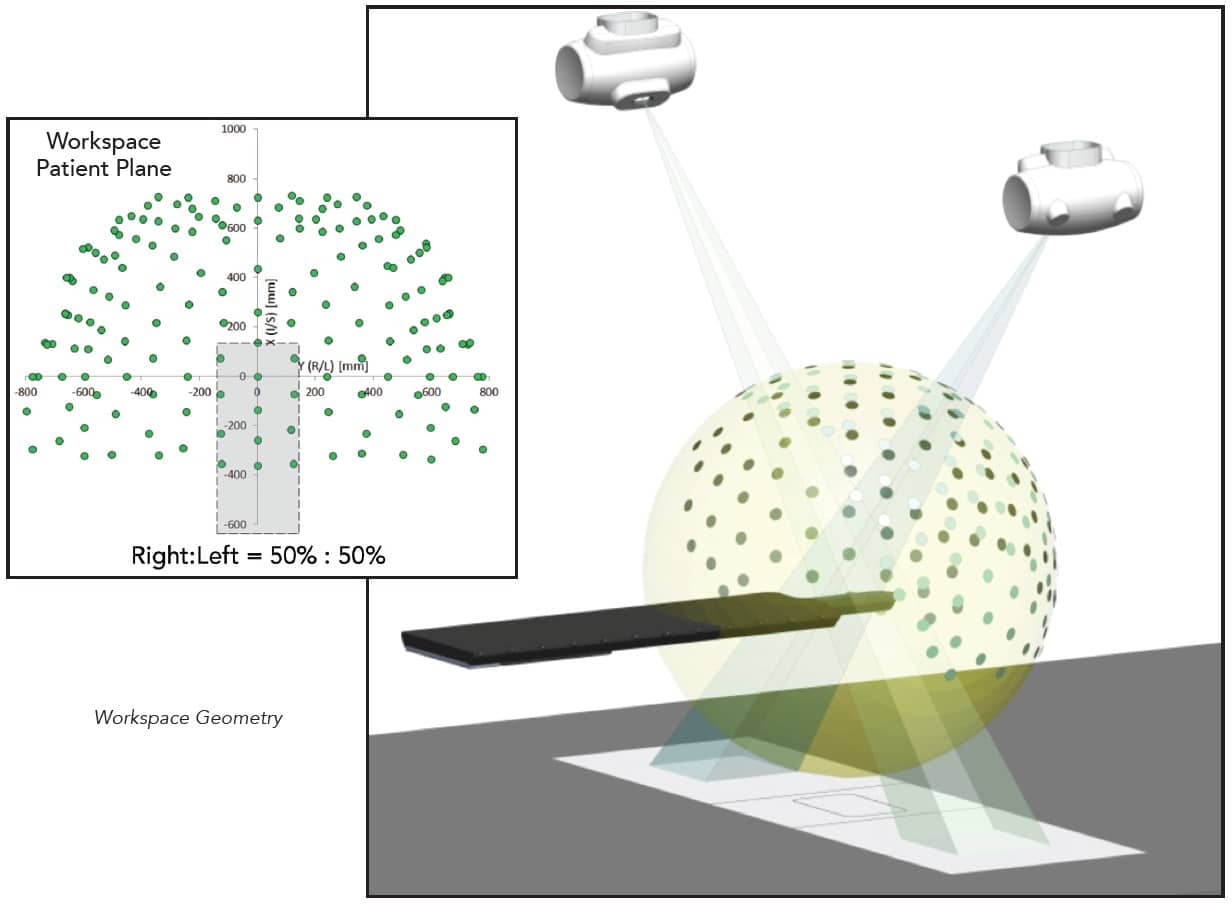
В пол рядом с операционным столом встроена пара рентгеновских детекторов размером 40 на 40 см, на базе йодида цезия, осажденного на кремниевый фотодиод. Вместе они генерируют стереоизображение разрешением 1024 на 1024 пикселя. Рентгеновскую визуализацию дополняет система из трех инфракрасных камер и LED-светодиодов, которые крепятся на кожу пациента. В сложных случаях перед операцией в опухоль вживляют дополнительные золотые маркеры, но, как правило, получается обойтись без них.
Отслеживая светодиоды, CyberKnife в режиме реального времени компенсирует дыхание и непроизвольные движения пациента. Общая точность системы составляет 0,42 ± 0,4 мм, а движения кожи пациента определяются с точностью до 0,35 мм.
Причем рентгеновские детекторы включаются лишь периодически, каждые 30–60 секунд. В остальное время CyberKnife полагается на компьютерную модель, которая описывает взаимосвязь между движениями опухоли и маркерами на поверхности тела.
Дополненная и виртуальная реальность
Из всех перечисленных нововведений, это наиболее близкое. Внедрение дополненной реальности в хирургию — дело ближайшего времени. Это логичное развитие интерфейсов роботов-хирургов, вопрос лишь в том, какую дополнительную информацию выводить в поле зрения врача.
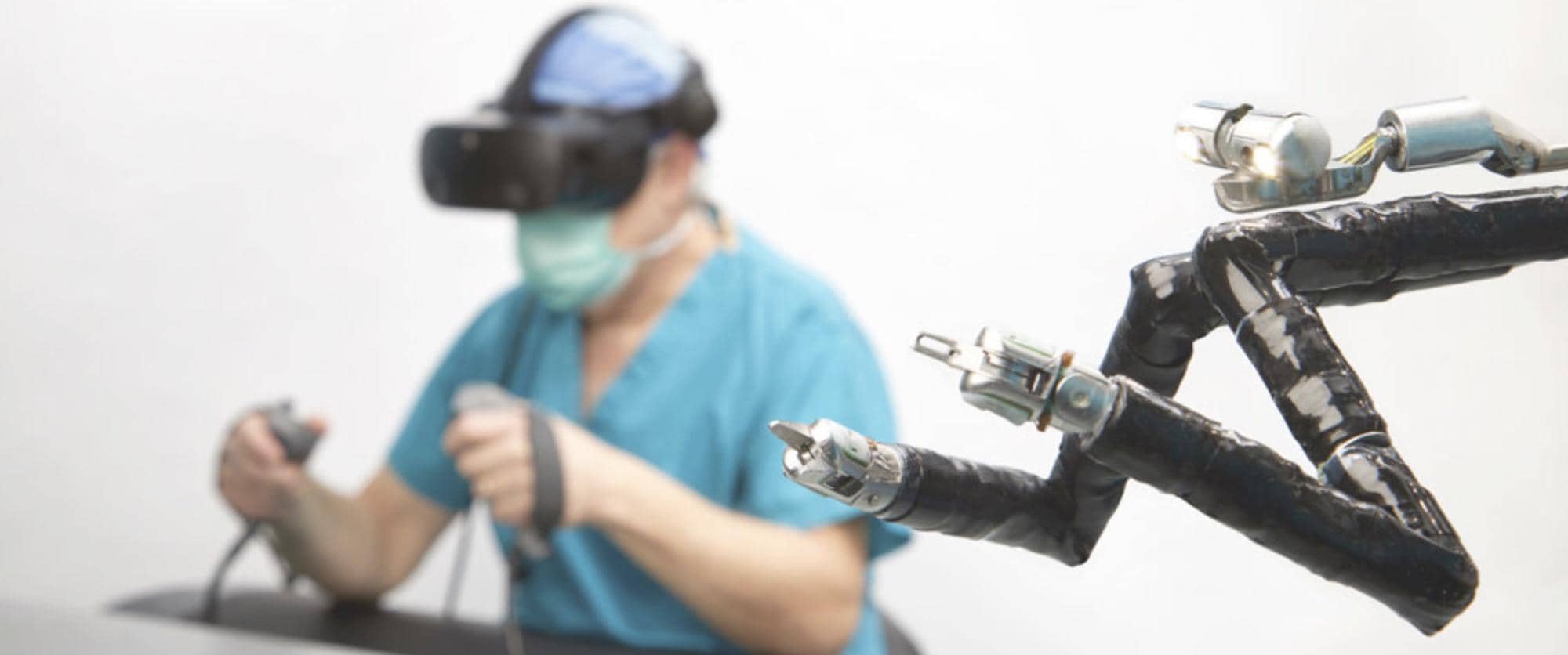
Более того, в декабре 2019 года в операционные официально пришла полноценная виртуальная реальность. FDA разрешило операции с использованием робота Vicarious Surgical.
Эта система воспроизводит воспроизводит человеческое тело: голову, плечи, локти и запястья. Робот подключается к современным очкам виртуальной реальности, так что хирург погружается в работу с головой. Притом, камера с манипуляторами в сложенном виде проходит через 1,5-сантиметровый разрез.
Вот она какая, по-настоящему иммерсивная хирургия.
Больше чем марионетки

В книжной и кино-фантастике не протолкнуться от роботов-хирургов и медицинских капсул, которые сами и диагноз поставят и операцию проведут. Как видите, в реальности до подобных устройств еще очень далеко. Быть может, мы вообще никогда не доверим роботам принятие медицинских решений и автономную хирургию.
Однако прямо сейчас Renishaw, Hansen Medical, Medrobotics, Transenterix, Think Surgical, Stryker, Mazor Robotics, Smith & Nephew, Medtech — десятки крупных компаний и стартапов разрабатывают и испытывают хирургические системы, которые вполне могут сниматься в фантастических фильмах. Они не заменят хирургов, но это не важно, главное — они помогут спасать реальные жизни в ближайшем будущем.
Если вам понравится прочитанное, заглядывайте в Santry's blog в Telegram — ведь я пишу не только лонгриды.
P.S. Благодарю Михаила Шалыгина — клинического специалиста из демонстрационно-обучающего центра da Vinci за помощь в подготовке материала.